Цели:
- Обучающая – обобщить знания учащихся об основных свойствах элементов-металлов и образуемых ими простых и сложных веществ.
- Воспитательная – воспитывать экологическую культуру (на примере последствий загрязнения окружающей среды тяжелыми металлами), ответственное отношение к собственному здоровью (в связи с необходимостью или вредом поступления в организм некоторых металлов).
- Развивающая – совершенствовать умения экспериментально подтверждать химические свойства веществ, на основе теоретических знаний, выполнять практические задания, выявлять существенное, делать выводы, устанавливать межпредметные связи, развивать экспериментальные умения, формировать мировоззренческие понятия о познаваемости природы.
Оборудование: компьютер, проектор, экран, презентация Power Point, периодическая система периодических элементов Д.И. Менделеева, коллекция металлов, Zn, HCl, Ni, CuSO4, Cu, H2SO4 концентрированная, Na, H2O, модели кристаллических решеток.
Тип урока: Урок обобщения и систематизации знаний.
Ход урока
Орг. начало и постановка целей урока.
Учитель биологии: Внимательно осмотритесь вокруг. Где бы вы ни были: дома или в школе, на улице или в транспорте – вы увидите, какое множество металлов трудится вокруг нас и для нас. Сегодня на уроке мы с вами вспомним всё, что мы узнали о металлах на уроках химии, географии, биологии и физики.
Постановка целей.
Активизация мыслительной деятельности учащихся.
- положение металлов в периодической системе
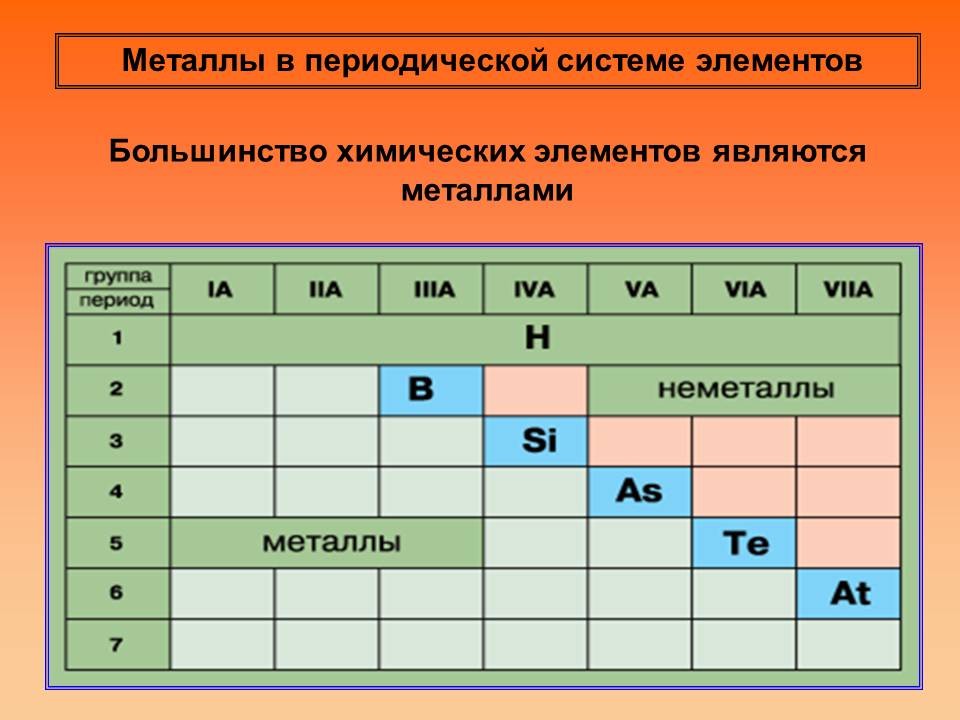
Учитель химии: Большинство химических элементов являются металлами.
Как расположены металлы в периодической системе?
(На экран выводится слайд “Положение металлов в Периодической системе Д.И. Менделеева)
Выступление учащегося: Если провести диагональ через бор и астат, то в нижнем левом углу будут расположены металлы, кроме инертных газов (показывает по таблице на слайде)

Учитель химии: А что ещё вам известно о металлах? Ответьте на несколько наших вопросов.
Интеллектуальная разминка: (вопросы на слайдах по три)
1. Выберите группу элементов, в которой находятся только металлы:
А) Al, As, P;
Б) Mg, Ca, Si;
В) K, Ca, Pb (В)
2. Металлический кальций проявляет свойства:
А) окислителя
Б) восстановителя;
В) окислителя или восстановителя в зависимости от условий. (Б)
3. Ионы какого металла входят в состав наиболее важных биологических веществ, таких как гемоглобин и хлорофилл? (железо)
4. Соединения, какого металла входят в состав дентина зубов, костей, отвечают за сворачиваемость крови и сокращение мышечных волокон? (кальций)
5. Основные продукты цветной металлургии:
А) медь и алюминий;
Б) сталь и медь;
в) железо и медь. (А)
6. Производство каких металлов есть в районе Норильска? (медь, никель, кобальт и др.)
Обобщающее повторение. Общие физические свойства металлов.
Учитель химии: Используя знания, полученные на уроках физики, химии, биологии, географии давайте вспомним о нахождении металлов в природе, особенностях их строения и физических свойствах.
1. Нахождение металлов в природе
Учитель химии: В природе металлы существуют как в свободном, так и в связанном виде. В свободном виде существуют малоактивные металлы: платина, золото, серебро. Но в основном металлы встречаются в виде различных соединений.
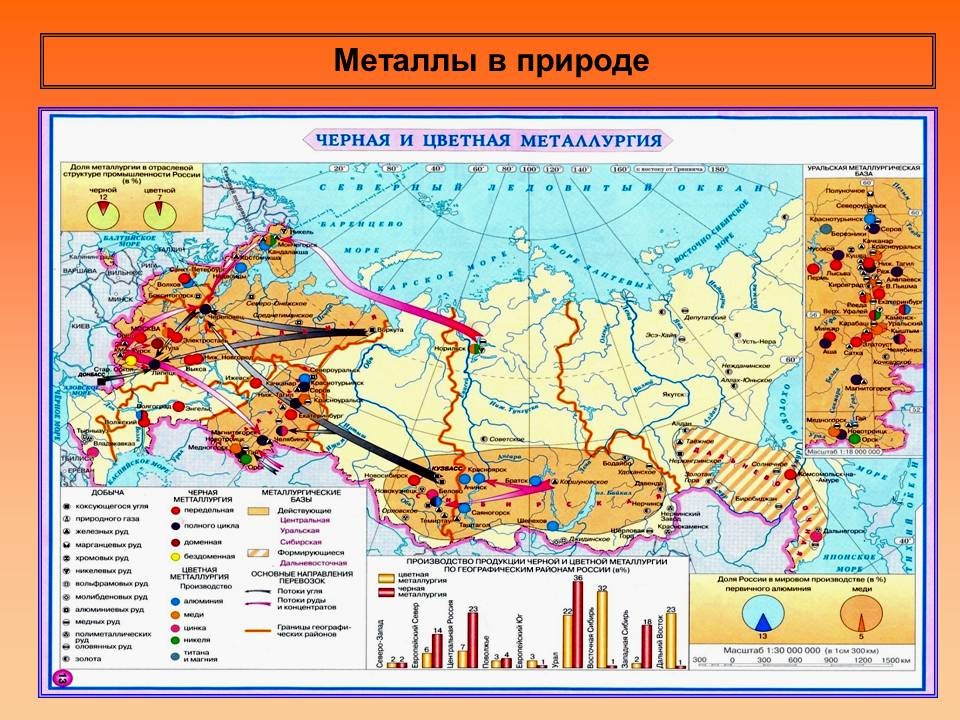
Учитель географии: В природе существует несколько десятков металлов, которые человек использует в разных хозяйственных целях. Производство этих металлов обеспечивает две отрасли: черная и цветная металлургия. Основу черной металлургии составляют руды содержащие соединения железа, а основу цветной металлургии – соединения таких металлов как медь, никель, кобальт и других.
Выступление учащегося: о расположении месторождений руд цветных и чёрных металлов.
В России три металлургических баз, где добывают и производят черные и цветные металлы: Уральская, Центральная, Сибирская и строящаяся база Дальневосточная.
На территории Центральной базы добывают руды таких металлов как железо, никель, алюминий.
На территории Уральской базы сосредоточены запасы медных, алюминиевых, никелевых, урановых руд, золота, платины.
В Сибирской базе имеются месторождения алюминия, железа, полиметаллических руд, золота, меди, никеля, кобальта, платины. Основная добыча и производство меди, никеля, кобальта и платины ведется в районе Норильска, на основе Талнахского месторождения. Здесь производится до 90% Российского никеля и кобальта, 75% меди и 100% платины.
Учитель биологии: А знаете ли вы, что живые организмы, могут подсказывать человеку, где могут находиться те или иные залежи металлических руд? Например, это могут делать некоторые растения. Их называют рудознатцами. Они могут реагировать на присутствие в почвенном растворе солей тех или иных металлов изменением формы стеблей и листьев, окраской цветков. Так соли никеля обесцвечиваю цветки, а избыток меди вызывает появление в них синих и голубых тонов, например лепестки роз голубеют. Залежи железных руд угнетают древесную растительность, а остальные растения имеют яркие желто-зелёные листья.
2. Особенности строения (слайд о строении металлов, металлической связи)
Учитель химии: Каковы особенности строения металлов?

Выступление учащегося: об особенностях строения металлов
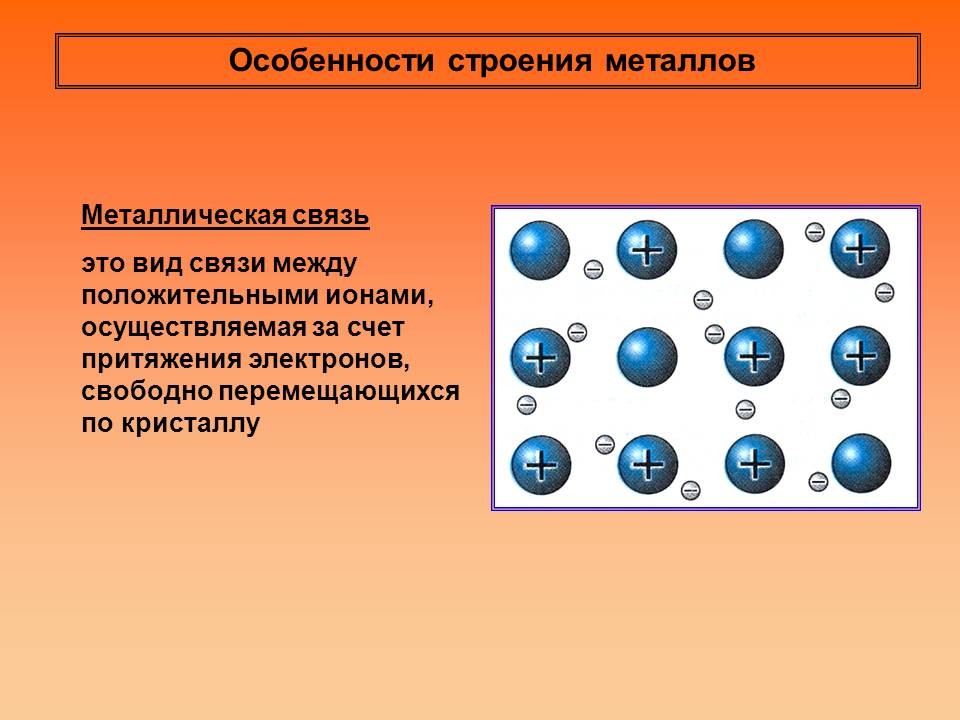
Атомы металлов имеют небольшое число валентных электронов. Они слабо связаны с ядром и могут легко отрываться от него. В результате в узлах кристаллической решетки появляются положительно заряженные ионы, а между ними свободно перемещаются электроны – образуется так называемый “электронный газ”.
Вид связи между положительными ионами, осуществляемой за счет притяжения электронов, свободно перемещающихся по кристаллу, называется металлической.
3. Физические свойства
Учитель химии:
Металлы имеют многие специфические свойства. Давайте вспомним, какими физическими свойствами обладают металлы?
(учащие проговаривают физические свойства металлов, которые затем демонстрируются на слайдах)
- При комнатной температуре металлы - твердые вещества, за исключением ртути
- Большинство металлов серебристо-серого цвета с разными оттенками, за исключением золота и меди
- Все металлы имеют характерный блеск, называемый металлическим блеском
- Металлы хорошо проводят тепло и электричество
- Металлы различаются по твердости
- Металлы значительно различаются по плотности и тяжести
- Металлы сильно различаются по температуре плавления.
- Металлы ковкие и пластичные
Общие химические свойства металлов.
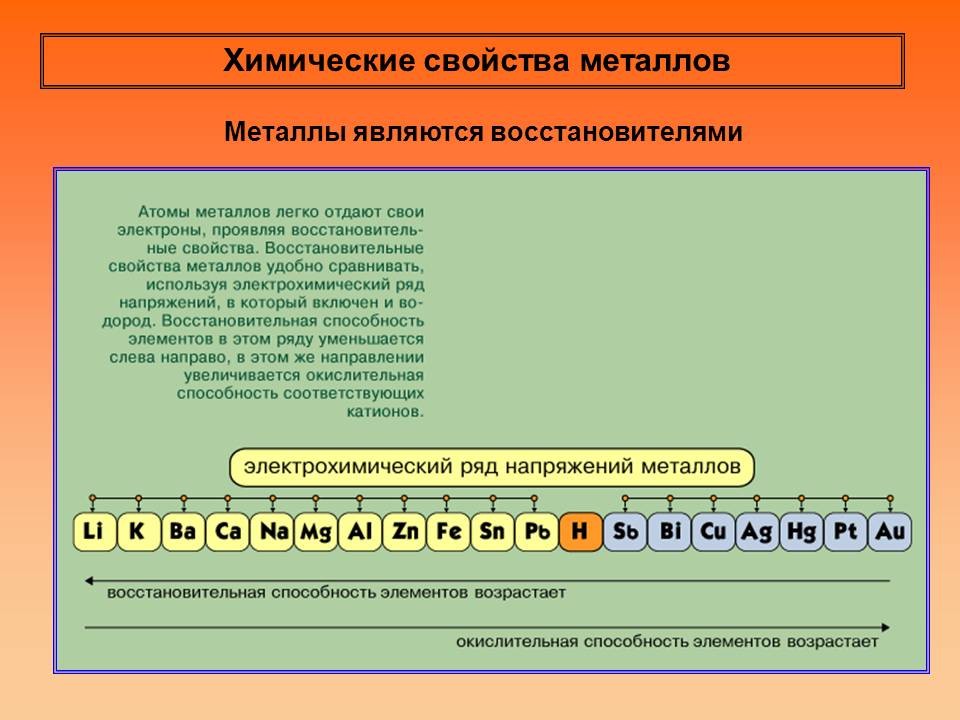
Учитель химии: Металлы являются восстановителями. Давайте вспомним, в реакциях с какими веществами металлы проявляют эти свойства?
На экран выводятся последовательно слайды, в ходе обсуждения учениками демонстрируются химические реакции и записываются их равнения на доске, подтверждающие свойства металлов.

Большинство металлов довольно хорошо реагирует с кислородом (за исключением золота, платины и серебра), образуя соответствующие оксиды:
2Fe + O2 = 2FeO
4Fe + 3O2 + 6H2O = 4Fe(OH)3
Взаимодействуют с серой, образуя сульфиды
Fe + S = FeS
Взаимодействие активного металла натрия с водой
2Na + 2H2O = 2NaOH + H2
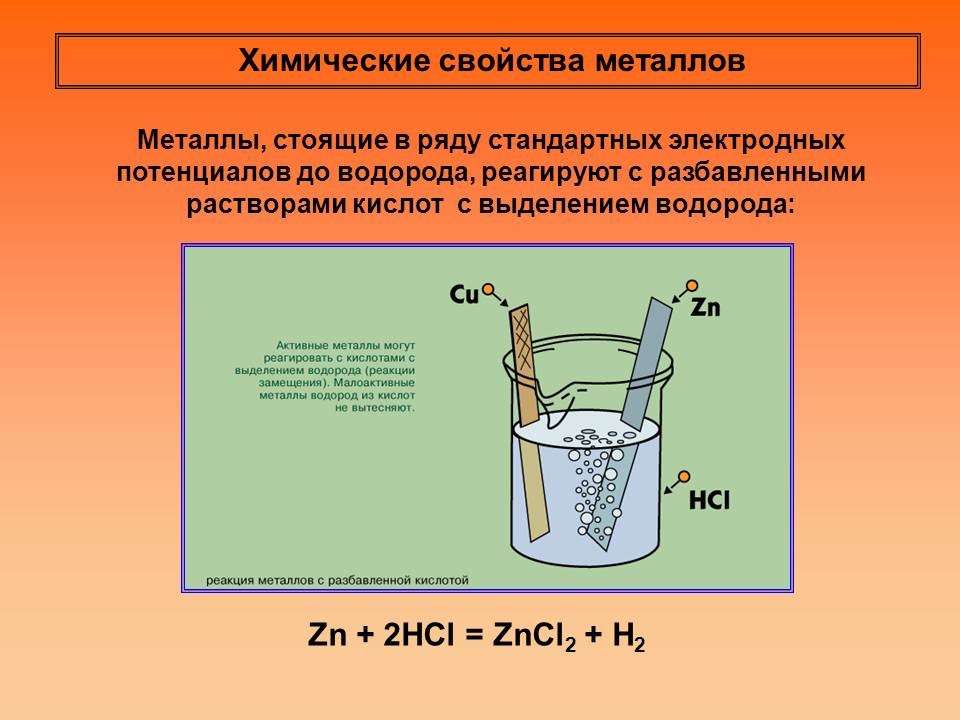
Металлы, стоящие в ряду стандартных электродных потенциалов до водорода, реагируют с разбавленными растворами кислот с выделением водорода:
Zn + 2HCl = ZnCl2 + H2
Металлы реагируют с растворами солей менее активных металлов, происходит реакция обмена
Fe + CuSO4 = FeSO4 + Cu
Металлы реагируют с кислотами-окислителями
Cu + 2H2SO4(конц) = CuSO4 + SO2
+ 2H2O
Биологические свойства металлов
Учитель биологии: Кроме выше перечисленных химических свойств, металлы, входя в состав внутриклеточной среды и сложных органических соединений организма, определяют их биологические свойства. Давайте вспомним некоторые из них, с которыми мы знакомились на уроках биологии.
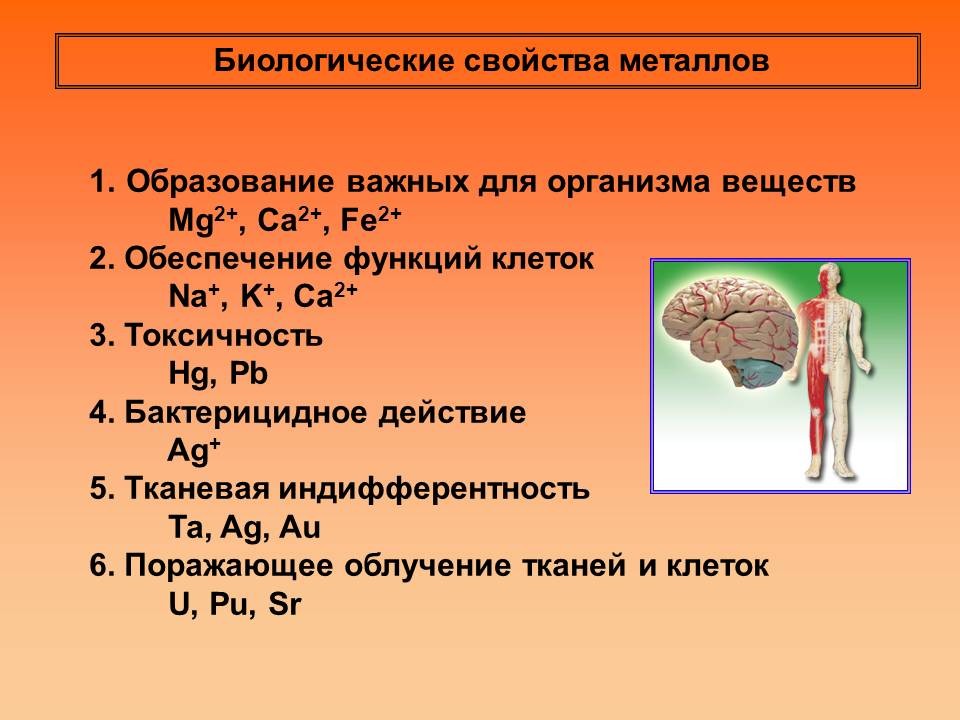
(учащие проговаривают биологические свойства металлов, который постепенно выводятся на слайде)
1. образование важных для организма веществ
Mg2+, Ca2+, Fe2+
2. обеспечение функций клеток
Na+, K+, Ca2+
3. токсичность
Hg, Pb
4. бактерицидное действие
Ag+
5. тканевая индифферентность
Ta, Ag, Au
6. поражающее облучение тканей и клеток
U, Pu, Sr
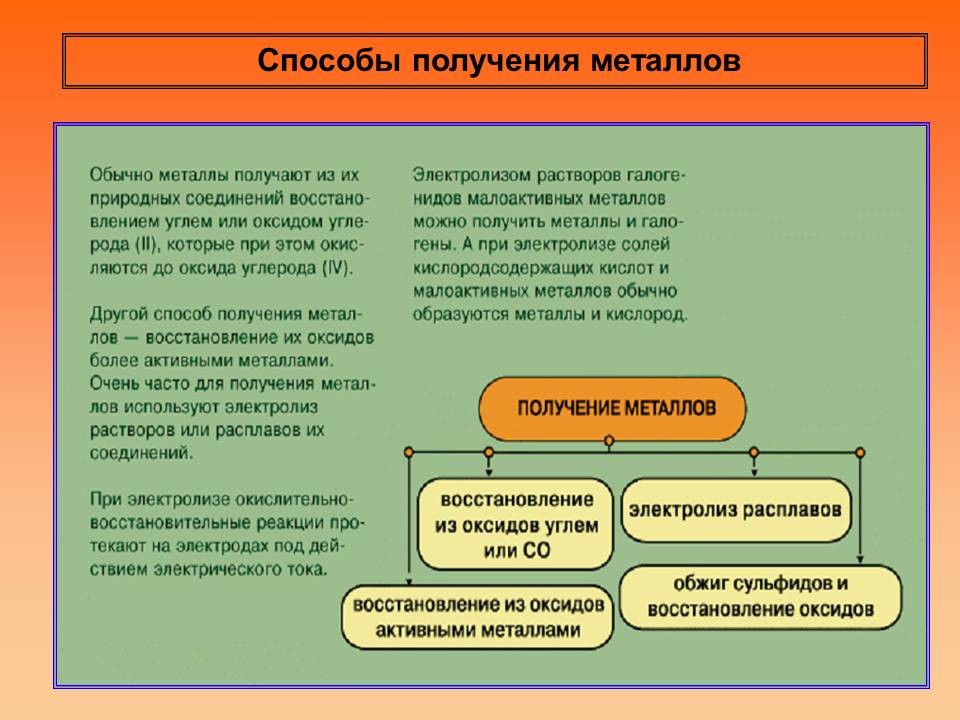
Способы получения металлов
Учитель химии: Существует несколько основных способов получения металлов.

Применение металлов и их сплавов, патологическое действие металлов и их соединений на организм человека
Учитель химии: Многие металлы способны реагировать друг с другом. Продукты взаимодействия металлов между собой называются сплавами, которые очень широко используются человеком в различных сферах хозяйственной деятельности. Многие предметы, которыми мы ежедневно пользуемся, сделаны из металлов. Без металлов невозможен технический прогресс.
(на экран выводятся последовательно слады применения металлов)
Учитель биологии: Но параллельно уживаются польза от применения металлов и опасность от многих из них для живых организмов. Даже ионы металлов, которые обычно обеспечивают нормальную работоспособность организма, в избытке могут вызывать серьёзнейшие нарушения и заболевания.
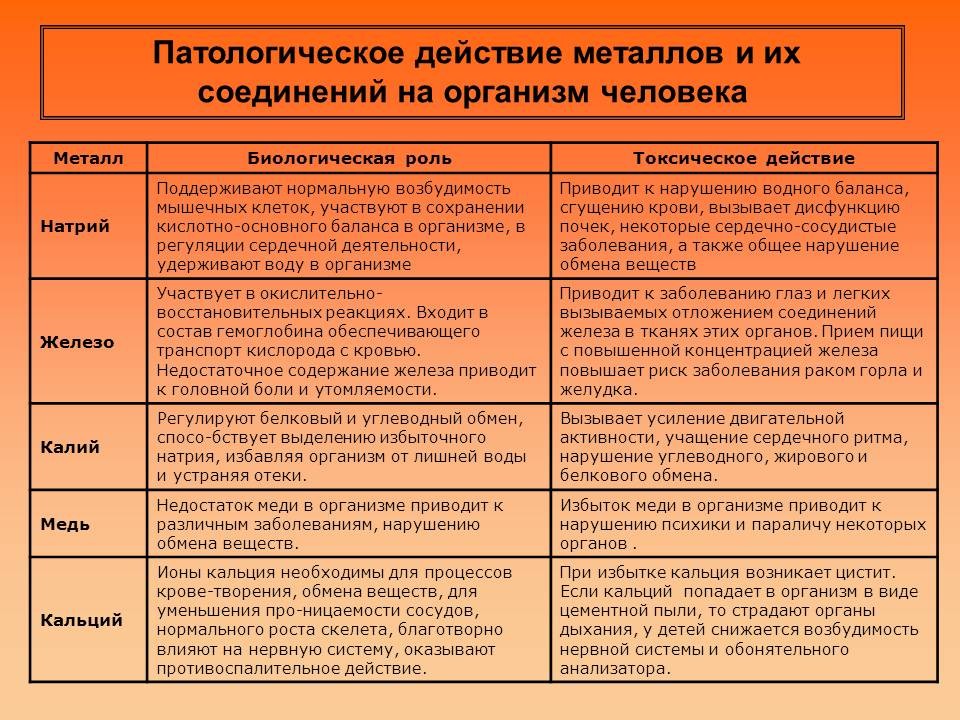
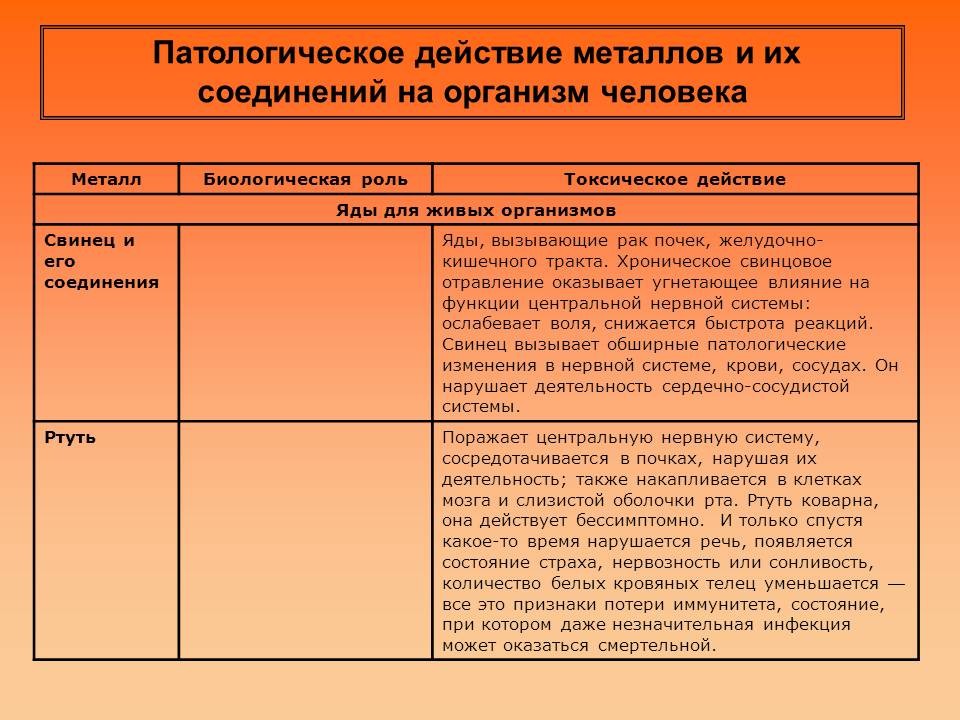
Выступление учащегося: о биологической роли и токсическом действии металлов на организме
Так железо, входящее в состав гемоглобина, важнейшего белка, обеспечивающего транспорт кислорода с кровью ко всем органам, при избытке поступления в организм приводит к заболеваниям глаз и лёгких, откладываясь в тканях этих органов. Ионы кальция, необходимые для процессов кроветворения и нормального роста скелета, при избытке вызывают такое заболевание как цистит. Недостаток ионов меди в организме приводит к различным заболеваниям, нарушению обмена веществ. Однако избыток меди в организме приводит к нарушению психики и параличу некоторых органов.
Соединения таких тяжёлых металлов как свинец и ртуть, попадая в организм вместе с пищей и водой вызывают сильнейшие отравления, проявляющиеся в поражении центральной нервной системы, почек, сосудов, крови. Происходят нарушения деятельности сердечно-сосудистой системы, снижение иммунитета.
VIII. Итоговое тестирование
1. У какого элемента ярче выражены металлические свойства и почему?
А) Na; Б) K; В) Rb; Г) Cs. (Г)
2. Найдите электронное уравнение, соответствующее данной схеме реакции: Ca+ Br2 —> CaBr2
А) Br 20+2e- >2 Br –;
Б) Br 20+2e- >Br2 –;
В) 2Br- - 2e- >Br 20 (А)
3. Какой металл не входит в состав руд, добываемых на Талнахском месторождении в районе г. Норильска?
А) никель; Б) алюминий; В) медь; Г) кобальт. (Б)
4. Основные продукты черной металлургии:
А) алюминий и сталь; Б) сталь и чугун; В) чугун и алюминий. (Б)
5. Присутствие руд какого металла в почве вызывает обесцвечивание цветков у растений, растущих на таких территориях:
А) меди; Б) железа; В) никеля; Г) цинка (В)
6. Ионы какого металла, составляя физиологическую основу внутренней среды организма, в избытке могут вызывать нарушение водного баланса, сгущение крови, некоторые сердечно-сосудистые заболевания:
А) магния; Б) кальция; В) калия; Г) натрия (Г)
Подведение итогов урока
Задание на дом
Химия
- Повторить параграф 11-14 по учебнику О.С. Габриеляна, упр. 6, стр. 75, упр. 4-6, стр. 82-83
Биология
- Повторить параграф 1.1 по учебнику А.А.Каменского