Базовый уровень. Учебник Кузнецова Н.Е., Гара Н.Н.
Цель: организовать проблемно-исследовательскую деятельность на уроке для развития универсальных учебных действий учеников в процессе изучения свойств и применения многоатомных спиртов.
Учебные задачи, направленные на достижение результатов:
- личностных: сформировать познавательный интерес на основе положительной мотивации к обучению;
- метапредметных: устанавливать причинно-следственные связи; принимать решения в проблемной ситуации, задавать вопросы, необходимые для организации собственной деятельности и сотрудничества с партнёром; проводить химический эксперимент и исследование;
- предметных: характеризовать свойства и особенности строения многоатомных спиртов, их практическую значимость; находить информацию в дополнительных информационных источниках.
Реактивы: вода, растворы сульфата меди (II), гидроксида натрия, глицерин. раствор соляной кислоты, индикатор метиловый оранжевый; этиленгликоль, натрий, этиловый спирт, раствор куриного белка, перманганат калия.
Форма урока: проблемно-исследовательская.
Эпиграф:
«Если у меня есть тысяча идей, и только одна из них оказывается плодотворной, я доволен.»
Альфред Нобель
План урока
1. Взаимопроверка учащихся по группам (класс делится на 4 группы, каждая группа задает вопросы по кругу по теме «Одноатомные спирты», ребята заранее готовят по 5 вопросов соперникам, они должны быть оригинальные, но в пределах программы, можно маленькие цепочки превращений, устные задачи), в зависимости от сложности отвечающие могут получить от 1 до 5 баллов. У каждой группы лист достижений (Приложение 1).
2. Изучение нового материала.
Почему эпиграфом нашего урока служат слова Нобеля?
В 1779 г. шведский аптекарь-химик Карл Шееле впервые получил глицерин и назвал полученную жидкость «сладкое масло». Это трехатомный спирт - глицерин.
Составьте формулу этого вещества.
Этиленгликоль впервые был получен в 1859 году французским химиком Вюрцем из диацетата этиленгликоля омылением гидроксидом калия и в 1860-м гидратацией этиленоксида. Он не находил широкого применения до Первой мировой войны, когда в Германии его стали получать из дихлорэтана для использования в качестве замены глицерина при производстве взрывчатых веществ.
Составьте формулу этого спирта.
- Почему наши соединения – это спирты?
- Сформулируйте тему урока.
- Сформулируйте цель.
- По какому плану изучают вещества? (План дается заранее на первых уроках в 10 классе).
3. Изомерия и номенклатура двух- и трёхатомных спиртов. Читаем параграф. Даем названия другим спиртам.
![]()
4. Физические свойства.
Ребята, перед вами пробирки с глицерином и этиленгликолем. Рассмотрите, что представляет собой эти вещества. Опишите их физические свойства.
Растворимость глицерина и этиленгликоля в воде.
Лабораторный опыт по группам. К одному мл воды в пробирке прилейте равный объем глицерина и этиленгликоля и взболтайте смесь. Затем добавьте еще столько же спирта. Что можно сказать о растворимости в воде? Опишите свойства, которые вы наблюдаете.
Добавлю, что эти физические свойства присущи и другим многоатомным спиртам. Надо помнить! Этиленгликоль очень ядовитое вещество!
Задание: сравните физические свойства многоатомных и одноатомных спиртов.
Подумайте о причине различия физических свойств одноатомных и многоатомных спиртов? Каковы изменения в относительных молекулярных массах спиртов? Каковы причины резкого различия температуры кипения?
Сделайте вывод о влиянии числа гидроксильных групп на физические свойства.
5. Химические свойства.
Какие химические свойства характерные для одноатомных спиртов?
Проблемный вопрос. А будут ли эти свойства характерны для многоатомных спиртов?
Лабораторный опыт №1
Взаимодействие глицерина и этиленгликоля с натрием:
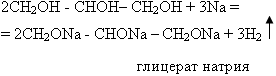
![]()
Лабораторный опыт №2
Взаимодействие глицерина и этиленгликоля с галогеноводородными кислотами: в пробирку налили соляной кислоты и добавили метиловый оранжевый. Далее прилили раствор глицерина в другую этиленгликоля до изменения окраски (происходит замещение гидроксогрупп).
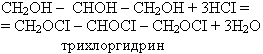
С этиленгликолем запишите сами.
Сделайте вывод: как вещества, содержащие гидроксогруппы, многоатомные спирты имеют сходные свойства с одноатомными спиртами.
Проблемный вопрос. Должно ли вызвать появление новых химических свойств увеличение числа гидроксогрупп в молекулах многоатомных спиртов?
Лабораторный опыт №3
1. К двум мл раствора щелочи в пробирке прибавьте несколько капель раствора сульфата меди (II). Что наблюдаете? Напишите уравнение реакции. Ученик записывает уравнение на доске, а учащиеся в тетрадях.
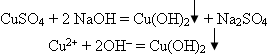
Наблюдали образование синего осадка гидроксида меди (II).
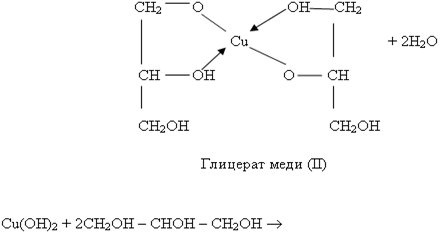
2. К образовавшемуся осадку гидроксида меди (II) прилейте глицерин и этиленгликоль смесь встряхните. Какие изменения произошли?
Учитель. Это качественная реакция на многоатомные спирты.
Лабораторный опыт №4
Изучение физиологического действия этанола, глицерина на белок куриного яйца.
Задание: провести лабораторный опыт «Изучение физиологического действия этанола, глицерина, этиленгликоля на белок куриного яйца».
Для этого в пробирку с 1 мл. куриного белка добавьте этанол, а в другую пробирку с 1 мл куриного белка добавьте этиленгликоль, в 3 пробирку глицерин.
Зафиксировать результаты опыта и продемонстрировать всем обучающимся.
Окисление многоатомных спиртов
Данная реакция получила название «вулкан Шееле».
Демонстрационный опыт в упрощенном виде:
![]()
Почему многоатомные спирты так окисляются?
Вывод: на примере многоатомных спиртов мы убеждаемся в том, что количественные изменения переходят в изменения качественные: накопление гидроксильных групп в молекуле обусловило в результате их взаимного влияния появление у спиртов новых свойств по сравнению с одноатомными.
Получение многоатомных спиртов (можно пользоваться интернетом)
А теперь каждая группа предложит свои способы получения многоатомных спиртов, если реакции повторяются группа получает по 1 баллу, если есть реакции только у одной группы получает 3 балла.
И самое главное применение глицерина и этиленгликоля (можно пользоваться интернетом). Каждая группа предлагает свои области, если применения повторяются -1 балл, если есть только у одной группы 3 балла.
Подведение итогов
Рефлексия.
Ответьте на вопросы:
- Что нового вы узнали сегодня на уроке.
- Было ли вам интересно.
- Где пригодятся знания сегоднешнего урока вам в жизни.
Домашнее задание.
Приложение №1
Номер группы |
Баллы за ответы по повторению |
Ответы на вопросы учителя |
Получение многоатомных спиртов |
Применение |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Приложение №2
Лабораторные опыты.
1. К одному мл воды в пробирке прилейте равный объем глицерина и этиленгликоля и взболтайте смесь. Затем добавьте еще столько же спирта. Что можно сказать о растворимости в воде? Опишите свойства, которые вы наблюдаете.
2. В пробирку налили соляной кислоты и добавили метиловый оранжевый. Далее прилили раствор глицерина в другую этиленгликоля до изменения окраски.
3. К двум мл раствора щелочи в пробирке прибавьте несколько капель раствора сульфата меди (II). Что наблюдаете? К образовавшемуся осадку гидроксида меди (II) прилейте глицерин и этиленгликоль смесь встряхните. Какие изменения произошли?
4. В пробирку с 1 мл. куриного белка добавьте этанол, а в другую пробирку с 1 мл куриного белка добавьте этиленгликоль, в 3 пробирку глицерин.