Тип урока: урок самостоятельного изучения материала.
Вид урока: урок-конференция с ролевыми фрагментами.
Цель урока: расширить представление о воде как уникальном веществе на Земле; экспериментальным путем изучить свойства воды как универсального растворителя; изучить аномальные свойства воды.
Задачи:
обучения:
- формировать умение сравнивать свойства веществ и находить причины сходства и различия;
- совершенствовать практические умения при работе с химическим оборудованием и реактивами;
- учить самостоятельно находить необходимый материал к изучаемой теме.
развития:
- информационной культуры – анализировать информацию, критически ее оценивать, обобщать, творчески перерабатывать;
- логических операций мышления при обобщении знаний;
- умения делать логические выводы из наблюдений по опыту.
воспитания:
- убежденности в позитивной роли химии в жизни современного общества, необходимости химически грамотного отношения к своему здоровью;
- коммуникативной компетентности (культуру поведения и общения в процессе учебной деятельности, чувство гордости за совместный результат познавательной деятельности).
Ход урока
Вступительное слово учителя. (Презентация 1)
Вода – самое распространенное и удивительное соединение на земном шаре, не похожее по своим физико-химическим свойствам ни на одно природное вещество. Тысячи лет человек восхищается, любуется и наслаждается водой, а она, зародившись миллиарды лет назад, так перестроила первоначальный вид и климат Земли, что возникли условия для появления и развития жизни. Весь наш мир можно представить как гигантскую химическую лабораторию, в которой ежесекундно протекают химические реакции. Величайшим в мире химиком в этой лаборатории является вода. Без её участия не обходится ни один природный процесс: будь то образование новой горной породы, нового минерала или сложнейшая биохимическая реакция, протекающая в организме растения или животного.
Что такое вода – привычное для нас вещество или чудо природы?
Цель работы нашей конференции: доказать, что в обычном веществе можно обнаружить удивительные свойства.
Выступление группы историков. (Презентация 2)
Тысячи лет человек восхищается, любуется и наслаждается водой. И все это время, пользуясь водой, люди не переставали задумываться не только о ее происхождении, но и о ее составе и структуре.
Ученые многих стран мира штурмуют пока все еще неприступную крепость – структуру воды. Тетраэдрическая паутина ее в трехмерном пространстве создает ажурные ячейки, напоминающие соты. Это предложение ученые выдвинули сравнительно недавно, и, наверное, они правы, поскольку до сих пор этого никто не опроверг, но, что самое удивительное, никто и не доказал пока однозначность такой информации. Короткая запись – Н2О, а сколько трудов положено учеными разных стран ради того, чтобы установить состав воды!
А с чего все началось? Началось все это давно – 24 июня 1783 года французский химик А.Лавуазье пропустил водяные пары через раскаленный ружейный ствол и разложил воду на составные элементы – водород и кислород. Тем самым он впервые доказал, что вода – сложное вещество.
Современникам А.Лавуазье казалось, что природа воды наконец-то выяснена, ее состав известен, но время показало, что это были только первые шаги на долгом и трудном пути исследования свойств и строения воды. Англичане Генри Кавендиш и Джозеф Пристли синтезировали воду, сжигая водород в кислороде, тем самым они подтвердили состав воды.
Классическая формула воды была предложена в 1805 году А.Гумбольдтом и Ж.Гей-Люссаком.
Выступление группы химиков. (Презентация 3)
Вода – универсальный растворитель. Вода активно реагирует со многими металлами с выделением водорода
- 2Na + 2H2O = 2NaOH + H2 (бурно)
- 2K + 2H2O = 2KOH + H2 (бурно)
- 3Fe + 4H2O = 4H2 + Fe3O4 (только при нагревании)
Из неметаллов с водой реагируют, например, углерод и его водородное соединение (метан). Эти вещества гораздо менее активны, чем металлы, но все же способны реагировать с водой при высокой температуре.
- С + Н2О = Н2 + СО
- СН4 + 2Н2О = 4Н2 + СО2
Вода реагирует со многими оксидами металлов и неметаллов.
Растворимость веществ в воде зависит от температуры. Растворимость твердых веществ в воде увеличивается с повышением температуры, а растворимость газов – уменьшается, поэтому воду можно почти полностью освободить от растворенных в ней газов кипячением.
При взаимодействии основного оксида с водой, образуется щелочь, которую определяем с помощью индикатора.
Выполнение лабораторного опыта: «Взаимодействие металлов и оксидов металлов с водой».
Выступление группы физиков-химиков: аномалии воды. (Презентация 4)
Вода – привычное для нас вещество. И в то же время сколько в нем необычного! Свойства воды не подчиняются общим закономерностям. В её свойствах много отклонений, аномалий.
Аномалия первая. Ближайшие родственники воды – сероводород, селеноводород, теллуроводород – представляют собой газы, которые имеют температуры кипения и плавления ниже 0oС. Вода плавится и кипит при значительно более высоких температурах. Известно, что на температуру кипения и плавления вещества оказывает влияние его относительная молекулярная масса: с увеличением её повышаются температуры кипения и плавления.
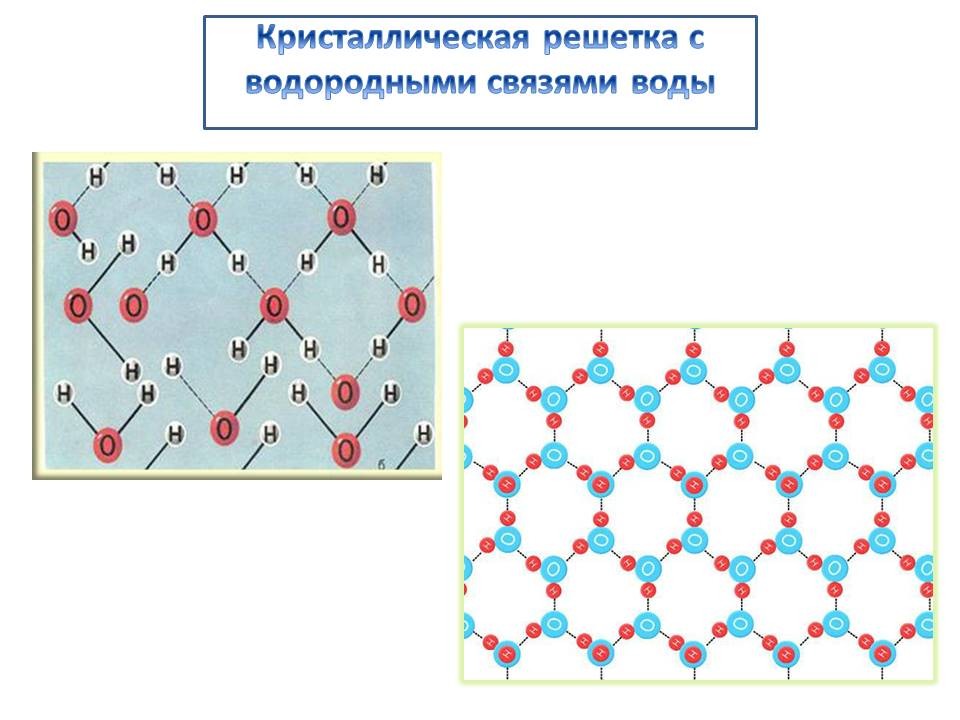
Из четырех веществ (Н2О, H2S, H2Se, H2Te) вода имеет наименьшую относительную молекулярную массу, но температуры плавления и кипения у неё наивысшие. Эту аномалию можно объяснить тем, что молекулы воды способны сцепляться друг с другом. Атом кислорода одной молекулы притягивает атом водорода другой. Связь между молекулами воды называется водородной. За счет этой связи молекулы связываются друг с другом и образуют целые группы молекул. Это затрудняет испарение воды, а следовательно, повышает температуру плавления и кипения.
Аномалия вторая. В 1913 году печальное известие облетело весь мир. Погиб, столкнувшись с айсбергом, гигантский океанский лайнер «Титаник». По-разному объяснили эксперты причины катастрофы. Сошлись на том, что в тумане капитан не разглядел огромную плавающую ледяную гору и, налетев на нее, корабль окончил свое земное существование.
Если мы посмотрим на это прискорбное событие глазами химика, то придем к весьма неожиданному выводу: «Титаник» пал жертвой еще одной аномалии воды. Устрашающие ледяные глыбы – айсберги – плавают, подобно пробке, на поверхности воды. Глыбы в десятки тысяч тонн. И все потому, что лед легче воды.
Попробуйте расплавить любой металл и в расплав бросить того же металла: он моментально утонет. Твердое состояние любого вещества имеет большую плотность, чем жидкое. Лед и вода – удивительное исключение из этого правила. Не будь этого исключения, все водоемы средних широт быстро промерзли бы до дна: все живое бы погибло.
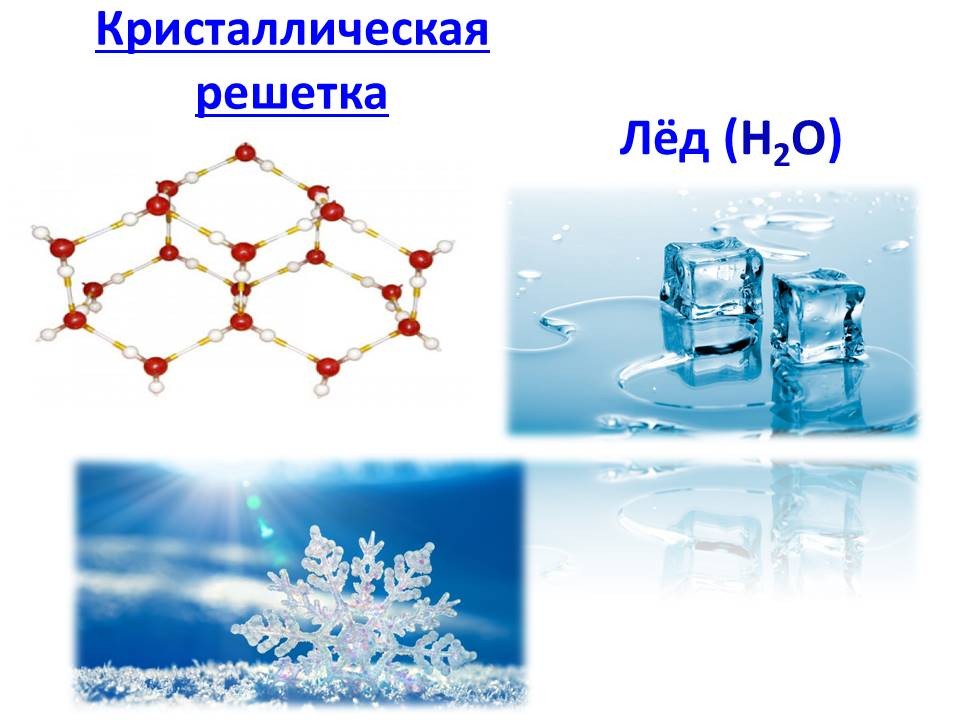
Вода – единственное вещество, которое при затвердевании расширяется. Поэтому плотность льда меньше плотности жидкой воды. Вот почему лед плавает на поверхности воды. Один кубический дециметр воды при 40С имеет массу 1000 г, а кубический дециметр льда – 916 г, то есть замерзшая вода увеличивает свой объем на одну десятую часть. Эту аномалию воды можно объяснить тем, что с понижением температуры увеличивается число водородных связей между молекулами. Это приводит к такому расположению молекул воды относительно друг друга, при котором образуются пустоты между молекулами. Кристаллическая решетка льда имеет ажурное строение.
Аномалия третья. Самое привычное для нас состояние воды – жидкое. Однако из того, что температура кипения воды – её аномальное свойство, следует, что в условиях Земли жидкое и твердое состояния её – также аномалия. Нормальным должно быть только газообразное состояние. Невозможным жителям невозможного мира, в котором все свойства воды были бы нормальными, пришлось бы строить специальные машины, чтобы сжимать такую воду, подобно тому как это делаем мы, получая жидкий кислород. Самое обычное свойство воды оказывается необычным и удивительным, если как следует с ним познакомиться и разобраться.
Аномалия четвёртая. Наличие водородных связей между молекулами затрудняет испарение воды, поэтому у неё очень высокая теплота испарения. Солнце – великий энергетик – нагревает воду всюду, где она есть: в луже, в пруду, в море, в океане. Вода поглощает в своем тонком слое почти всю энергию падающих в неё солнечных лучей и испаряется. Необходимо очень много солнечной энергии, чтобы разъединить молекулы воды и превратить её в пар. Нет ни одного вещества, у которого бы удельная теплота испарения была бы больше, чем у воды. Метеорологи подсчитали, что Солнце испаряет на Земле за 1 минуту миллиард тонн воды. Энергия Солнца, поднятая с водяным паром вверх, неминуемо должна выделиться обратно. Каждую минуту водяной пар отдает атмосфере Земли огромное количество энергии – 2,2*1018 Дж. Столько энергии за то же время могли бы выработать 40 млн. электростанций, по миллиону киловатт каждая. Эта энергия переходит в тепловую, нагревая воздух. Это та энергия, которая переносит сотни миллиардов тонн воды по воздуху в облаках и орошает дождями всю поверхность Земли, за счёт неё дуют ветры, возникают бури, рождаются штормы и ураганы.
Аномалия пятая. В кристаллах льда, как и в жидкой воде, каждая молекула воды связана водородными связями с четырьмя соседними. Поэтому при плавлении льда приходится затрачивать большую энергию. Вода имеет большую теплоту плавления. Удельная теплота плавления льда 335 Дж на 1 г. Когда наступает зима, образуется лёд, вода отдает энергию, поглощенную при плавлении льда, обратно, подогревая землю и воздух. 1 литр воды, превращаясь в лед, подогревает на 10С 250 тысяч литров воздуха. Это смягчает переход к суровой зиме, сильным морозам. Вы радуетесь приходу весны, восхищаетесь прекрасными деньками золотой осени. Радостная весенняя капель и багряный убор лесов – эти поэтические образы мира рождены водой.
Аномалия шестая. У воды самое высокое поверхностное натяжение из всех жидкостей, кроме ртути. Поверхность воды всегда затянута тончайшей пленкой из молекул, прочно связанных водородными связями. По ней, как по гамаку, бегают водомерки. Силы поверхностного натяжения заставляют воду подниматься из глубины почвы и питать растения. Вода сама поднимается вверх, по капиллярным сосудам стволов деревьев и стеблям трав, доставляя растворимые вещества на большую высоту от корней к листьям и плодам.
Аномалия седьмая. Вода – самое распространенное вещество на Земле. В ней растворены газы атмосферного воздуха: азот, кислород, углекислый газ. В ней растворены сотни различных соединений почти всех элементов периодической системы. В ней взвешены мельчайшие частицы пыли. Это мы и называем чистой водой. Растворенные в воде соли придают ей приятный вкус. В воде некоторых источников содержится большое количество растворенных веществ. И она имеет целебные свойства. Это минеральная вода.
Аномалия восьмая. 2018 год. Олимпиада в Пхёнчхане. Как великолепно искусство 15-летней Алины Загитовой. И здесь мы вспоминаем об аномалии воды, связанной со свойствами именно кристаллической модификации этого вещества; об аномальном изменении свойств льда с изменением давления. Спортсменка так легко катится по льду потому, что под давлением, которое оказывают на лед лезвия коньков, лед плавится и образующаяся жидкая вода является великолепной смазкой. Об этом знают все. Но не все знают, что этого быть не должно. Потому что практически у всех других веществ при повышении давления температура плавления не понижается, а повышается. У воды же наоборот: понижение давления ведет ведёт к понижению температуры плавления льда.
Выступление группы экологов. (Презентация 5)
Большая часть воды на Земле сосредоточена в морях и океанах, второе место по объему водных масс занимают подземные воды, третье – лед и снег. Поверхностные воды суши, атмосферные и биологически связанные воды составляют доли процента от общего объема воды гидросферы.
Мертвые долины и скалы оживают только от воды. Почти все мифы древних народов рассказывают о том, что живой мир возник из воды. И древние человеческие цивилизации возникали и процветали прежде всего вдоль великих рек: Нила, Ганга, Хуанхэ, Тигра и Евфрата, Дуная и Рейна, Волги, Дона и Днепра.
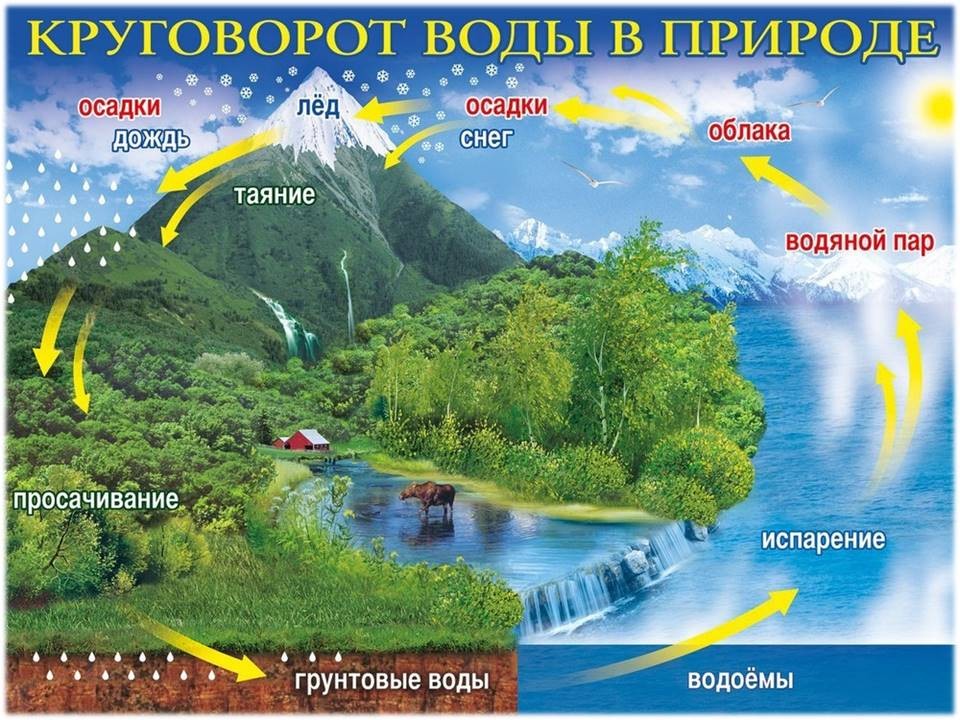
Вода совершает в природе два круговорота. Большой круг: из океанов, морей, рек и водоемов вода испаряется в атмосферу, конденсируется в облака и дождем выпадает на землю и с реками – опять в океан. И малый круг: растения всасывают воду из земли, с зеленью и фруктами вода попадает в тело животных и человека, откуда снова возвращается с выделениями и дыханием в воздух и в землю. Благодаря такому круговороту животные, растения и человек могут обитать на суше и все же оставаться водными существами, так как вода составляет основную среду всякого живого организма.
Мозг человека содержит 81% воды, в крови на 5 л приходится почти 4 л воды, в костях – 30% воды, в хрящах – 60%, в печени – 70%, в мышцах – 50-75%, в почках – 83%.
Высохшая мумия человека весит только 8 кг.
В сутки человек выделяет 3 л воды. Столько же ее нужно и вводить в организм. В это количество входит и вода, поглощаемая человеком с пищей. Нет ни одного продукта питания, в котором бы не было воды. В хлебе – 40% воды, в яйцах – 65%, в мясе – 75%, в рыбе – 80%, в молоке – 87%, в овощах – 90% (а в огурцах – 98%!).
У живых организмов в воде большая потребность. Так, подсолнух высотой с человека нуждается в 1 л воды, тридцатилетняя береза – в 60 л, а высокий хмель высасывает 300 л воды в день.
Высокое содержание воды в клетке – самое необходимое условие ее жизнедеятельности и зависит от интенсивности процессов обмена веществ. Так, в быстрорастущих клетках зародышей человека и животных содержится около 95% воды, в клетках молодого организма – 70-80%, а к старости – значительно снижается.
Роль воды в клетке – велика и многогранна. Она определяет объем и упругость клетки. В ней не только протекают химические реакции обменных процессов, но она сама участвует во многих из них. Из воды и углекислого газа в результате фотосинтеза образуется крахмал. Она выполняет терморегулирующие функции в организме.
22 февраля 1993 года Генеральная Ассамблея Организации Объединённых наций объявила 22 марта Всемирным днём воды (водных ресурсов). К проведению Всемирного дня воды привлекаются правительства разных стран, международные агентства, общественные организации, учреждения образования и культуры с целью привлечение внимания к проблемам нехватки питьевой воды, необходимости сохранения и рационального использования водных ресурсов.
Заключительное слово учителя
Мы привыкли к воде, как привыкают к самым обычным явлениям – ведь она всегда с нами: в быту, на работе, в природе. Широкая распространенность воды породила представление о ней как о весьма простом теле. В течение многих веков ее принимали за элемент. Сейчас уже никто этого не скажет.
Вода – совершенно необыкновенный минерал прежде всего потому, что это самое известное и вместе с тем самое загадочное вещество. О воде, знакомой человеку с колыбели, написаны бесчисленные монографии, ученые продолжают изучать ее свойства. И тем не менее трудно найти другое вещество, в котором было бы спрятано столько труднообъяснимых качеств.
Необыкновенность физико-химических свойств молекул воды основана на способности их изменять структуру водородных связей. Эти связи легче разрушаются и быстро восстанавливаются. Между молекулами воды идет интенсивное взаимодействие, в результате происходит быстрое изменение их структурной решетки. Этим отличается структура молекул воды от других веществ, например твердых кристаллических тел, у которых существует устойчивая структурная решетка.
Необыкновенность свойств молекул воды – одна из важнейших основ сложных биохимических реакций, присущих процессам жизни на нашей планете. Вода – это действительно уникальное чудо нашей планеты.