Цели.
Образовательная: рассмотреть случаи применения I закона термодинамики; научить объяснять смысл I закона термодинамики.
Развивающая: развивать умения, моделировать и проводить мысленный эксперимент; устанавливать логическую взаимосвязь наблюдаемых явлений и состояние окружающей среды.
Воспитательная: воспитывать компетентность в сфере самостоятельной, познавательной деятельности студентов, основанная на условии и умении применять полученные знания в повседневной жизни.
Оборудование: электронные уроки, презентация, сборник задач.
Дидактические методы и приемы:
- Словесно-иллюстрированный.
- Дифференцированный подход к обучению студентов.
- Развитие творчества и самостоятельности.
- Контроль знаний и умений учащихся через тестирование.
Ход урока
I. Организационный момент (2 мин.)
II. Повторение изученного материала.
1. Фронтальный опрос:
- Что собой представляет закон сохранения энергии?
- Что такое внутренняя энергия?
- Как читается I закон термодинамики?
- Как рассчитывается количество теплоты, переданное системе?
- Что такое идеальный газ?
- Чему равна внутренняя энергия идеального газа?
2. На доске 3 учащихся решают задачи на изопроцессы. По графикам изопроцессов в координатных осях р, v (рис.1, 2, 3) постройте графики тех же изопроцессов в координатных осях P, T и V, T.
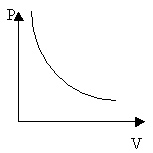
Рис. 1
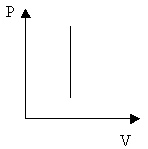
Рис. 2
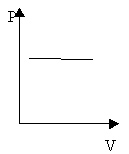
Рис.3
Повторяются изопроцессы. (Приложение 1)
III. Объяснение нового материала.
Используя первый закон термодинамики, рассмотрим различные процессы в газах, сопровождающиеся изменениями внутренней энергии.
1. Изотермический процесс: T-const.
При изотермическом расширении или сжатии газа его температура не изменяется:
![]() U=О
U=О
На основании I закона термодинамики при изотермическом расширении газа переданное количество теплоты равно работе совершенной газом.
Q=A
При изотермическом сжатии – работа внешних сил А¢ равна переданному количеству теплоты, взятому с противоположным знаком.
A' = -Q
2. Изобарный процесс: P – const.
В результате нагревания газа происходит увеличение его внутренней энергии и совершение работы расширения:
Q=![]() U+А
U+А
Q= ![]() U+РV
U+РV
Для того, чтобы давление газа при уменьшении объёма оставалось неизменным, газ нужно охладить, т.е количество теплоты. Понижение температуры газа при изобарном сжатии свидетельствует об уменьшении его внутренней энергии.
3. Изохорный процесс: V - const
При изохорном процессе работа газа равна нулю, поэтому изменения внутренней
энергии идеального газа равно полученному количеству теплоты. A=-A' =0.
![]() U=Q
U=Q
4. Адиабатный процесс: Q=0
Адиабатным называется процесс без изменения объёма и давления газа при отсутствии теплообмена с окружающими телами.
В соответствии с I законом термодинамики при адиабатном сжатии изменения внутренней энергии газа равно работе внешних сил.
![]() U=A
U=A
Так как при работе внешних сил при сжатии газа работа положительна,
внутренняя энергия газа увеличивается, его температура повышается. При
адиабатном расширении газ совершает работу за счёт уменьшения внутренней
энергии: ![]() U=-A. Поэтому
температура газа при адиабатном расширении понижается.
U=-A. Поэтому
температура газа при адиабатном расширении понижается.
Поскольку при адиабатном сжатии температура газа повышается, давление газа с уменьшением объёма растёт быстрее, чем при изотермическом процессе. Понижение температуры газа при адиабатном расширении приводит к тому, что давление газа убывает быстрее, чем при изотермическом.
В природе и технике часто происходит процессы близкие к адиабатным.
Примером адиабатного процесса в природе является процесс, происходящий в земной атмосфере в летнее время.
Один учащийся делает сообщение об образовании облаков. (Приложение 3)
Второй учащийся делает сообщение о применении адиабатного процесса в технике. (Приложение 4)
IV. Закрепление
1. Что такое адиабатный процесс?
2. Где применяется адиабатный процесс?
3. Как меняется температура идеального газа при адиабатном процессе?
4. Как изменяется внутренняя энергия идеального газа при изобарном сжатии?
Решение задач:
1. Какую работу совершили над двумя молями идеального газа при его адиабатном сжатии, если его температура увеличилась на 20К.
2. Какое количество теплоты получит 2 кг гелия при изотермическом нагревании на 50 К.
3. Газ переходит из состояния 1 в состояние 2 следующим образом. Определите, пользуясь графиком, отдает или получает газ тепло?
Заполните в тетради таблицу (Приложение 2)
Учащимся предлагается тест на два варианта. (Приложение 5)
V. Домашнее задание.
Г.Я.Мякишев §81 (упр. 1, 2, 9)
Сообщение: использование тепла в будущем.