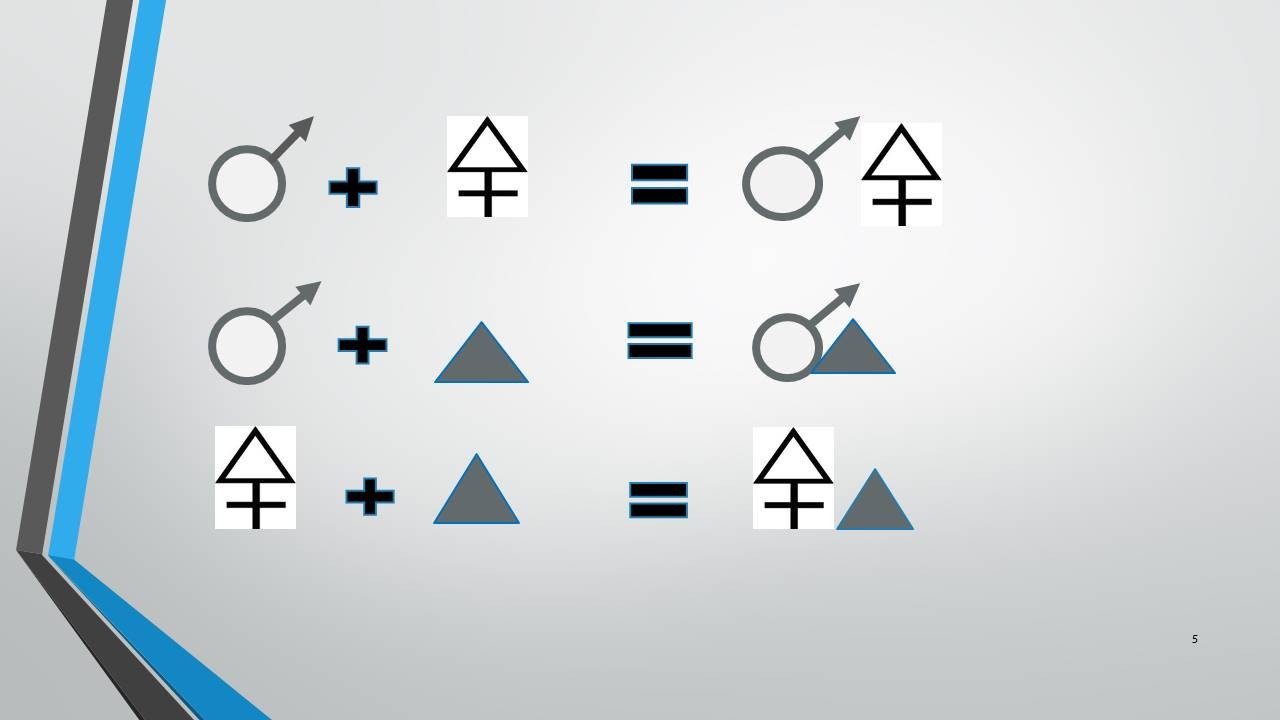Для нас наука естествознания – тот рычаг Архимеда, который
единственно способен повернуть весь мир к солнцу разума.
М. Горький
Цель вечера:Показать, что химия как часть естествознания (т.е. совокупности знаний о природных объектах, явлениях, процессах, а в наиболее правильном смысле – науки о Вселенной и законах её управляющих), является интегрированной и экспериментальной наукой.
Задачи вечера:
- Углубить, а также расширить знания учащихся о науке химии. Обогатить их память новыми знаниями и научными фактами.
- Развивать логическое мышление, познавательный интерес к науке химии. Формировать умения учащихся выполнять конкретные задания творчески и осмысленно.
- Формировать умения учащихся применять полученные знания. Развивать умения учащихся внимательно слушать и слышать других, делать правильные выводы.
- Воспитывать творческую любознательность. Воспитывать чувство бережного отношения к окружающему миру.
Средства для проведения вечера:
материальные:
- информационно-поисковые и справочные: «Стол источник знаний»:
- учебники химии 8-11 класс (разных авторов), дополнительная литература:
- Б. Н. Конарев Любознательным о химии Неорганическая химия. – Москва, Изд. «Химия» 1978.
- Е. Войскунский, И. Лукодьянов Ур сын Шама. – Изд. «Детская литература», 1975.И. А. Леенсон Удивительная химия. – М.: Изд-во НЦ ЭНАС, 2006.
- В. Рюмин Занимательная химия. – 8-е изд., испр., доп., перераб. – М.: Центрполиграф, 2015.
- Д. Шкурко Забавная химия. – Ленинград «Детская литература» 1976.
- В.И. Левашов Занимательная химия. – Государственное Учебно-педагогическое издательство Министерства просвещения РСФСР Москва 1962.
- Л.Е Сомин Увлекательная химия. – Москва «Просвещение» 1978.
- Фигуровский Н.А. История химии: Учеб. пособие для студентов пед. ин-тов по хим. и биол. спец. – М.: «Просвещение» 1979.
- Соловьев Ю.И. История химии: Развитие химии с древнейших времен до конца XIX в. Пособие для учителей. 2-е изд. – М.: «Просвещение» 1983.
- Энциклопедия школьника Неорганическая химия. – Москва Изд., «Советская энциклопедия» 1975.
- Энциклопедический словарь юного химика. Сост. В. А. Крицман, В. В. Станцо – М., «Педагогика» 1982.
- Б Ляпунов Химия всюду. – Москва Изд. «Детская литература» 1965.
- Периодические таблицы. Большую периодическую таблицу можно прикрепить на стену. Информационная карточка «Интернет-ресурсы»: www.lomonosov300.ru, www.smallbay.ru (история алхимии), www.chemlib.ru (библиотека по химии).
лабораторные: пульверизатор с раствором гексациано-(III) ферратом калия, смесь (NaHCO3 + сахарная пудра), (СН3СОО)2Pb(р-р), КNO3(конц.), Na2SiO3(р-р), KI(р-р), H2SO4(р-р), кристаллические соли: FeCI3, CuCI2, CoCI2, NiCI2, MnCI2, AICI3, FeCI2, (CН3COO)2Pb, тарелка с песком, фигурка, вырезанная из цинковой пластинки, полоски цинка, лучинка, спички, пробирки, большая колба, подставка, кирпич, предметное стекло, толстая нить, магнит, кисточка, утюг, электрическая плитка.
Подготовка к вечеру: Тема вечера сообщается заранее (примерно за два месяца). Необходимо создать пять групп, состоящих из учащихся 8–11 классов. Каждая группа работает по своей теме. Участники групп изучают дополнительную литературу, ищут интересные сведения по заданной теме, пишут тексты сообщений. Одна из групп очень тщательно готовится к проведению опытов под руководством учителя.
На занавесе сцены прикрепляется «чистый» ватман (на листе ватмана, акварельной кистью написано название естественно-научного вечера слабым раствором сульфата железа (III)). На втором листе ватмана обыкновенными красками написан план вечера, который открывается постепенно. План вечера можно демонстрировать на слайде.
Для ведения вечера учителем назначается два ведущих – учащиеся 11 класса.
Все стихи сочинила автор сценария О.И. Денисова.
План вечера:
Открытие первое:
«Удивительная и парадоксальная,
многогранная и таинственная,
древняя и молодая,
ищущая и созидающая,
военная, добывающая, новая,
весёлая, забавная, чудесная,
для кого-то скучная, трудная, нудная,
но, всё же очень интересная и нужная.
О ней говорят «тёмная», даже «чёрная».
«Искусством священным» считают её.
Эту науку кто-нибудь назовёт?»
Открытие второе: «Химическая тайнопись!»
Открытие третье: «Химическая … лингвистика!»
Открытие четвёртое: «Химические поучительные рассказы – загадки».
Открытие пятое: «Весёлая и занимательная химия».
Ход вечера
В зале слышны голоса участников вечера: Чему посвящён этот вечер? О чём этот вечер? Кто знает, что нас сегодня ждёт на этом вечере?
Первый ведущий (обращаясь ко всем участникам): Всем, добрый вечер! Мы понимаем ваше волнение и ваше нетерпение. Всем вам хочется узнать, что за вечер вас ожидает?
Второй ведущий (обращаясь ко всем участникам): Вы видите чистый лист ватмана. Но это вам только кажется. На самом деле на плакате написано название нашего вечера. Не верите? Предлагаю проверить. А потому приглашаем одного из вас на сцену.
(на сцену выходит участник).
Первый ведущий (обращаясь к участнику): Возьми пульверизатор и брызгай на ватман.
Голоса из зала: Какие-то надписи появляются! Ого! Синие буквы проявились! Вот это да!
Ведущие вместе (обращаясь ко всем участникам): Читаем вместе название: «Естественно-научный вечер «Удивительных открытий».
Голоса из зала: Что это за открытия? О чём мы сегодня узнаем?
Второй ведущий: Внимание на экран. (Читает стих), (слайд 2).
«Удивительная и парадоксальная,
многогранная и таинственная,
древняя и молодая,
ищущая и созидающая,
военная, добывающая, новая,
весёлая, забавная, чудесная,
для кого-то скучная, трудная, нудная,
но, всё же очень интересная и нужная.
О ней говорят «тёмная», даже «чёрная».
«Искусством священным» считают её.
Эту науку кто-нибудь назовёт?»
Голоса из зала, рассуждают: Однако этот стих о химии. Да-да, верно, о химии речь идёт. Точно, нам учитель рассказывал, что был в Древнем Египте город «Хем», значит «чёрный».
Первый ведущий: Да, вы правы! Эту науку зовут химия! Что же это за наука такая? Почему о ней все так по-разному выражают своё мнение?
Второй ведущий: Кто-то может рассказать всем нам об этой науке?
Голоса из зала: Мы можем!
Первый ведущий: Выходите на сцену.Мы все слушаем.
Участники поочерёдно выходят на сцену и начинают рассказывать.
Рассказ 1 (возникновение химии)
«Вначале я расскажу о том, как возникло само слово «химия»? Вообще единого мнения на этот счёт нет. Одни учёные связывают его с названием города «Хем» в Древнем Египте. В переводе это слово означает «чёрный», возможно потому, что почвы долины Нила были чёрного цвета. Другие исследователи берут за основу греческие слова «хюма» – «литьё», что наводит на мысль о процессе выплавки металла или «химевис», значит «смешивание». Наконец, ищут даже связи слова «химия» с древнекитайским «ки» – золото». На уроках мы говорили, что химия – это наука, изучающая вещества и их превращения, она является одной из важнейших отраслей естествознания. Ещё о химии можно сказать, что это древнейшая область человеческой деятельности. Посмотрим в глубь веков! Что мы видим? Человек использовал для своих нужд, то, что давала ему природа: жилища строил из дерева, орудия труда вначале делал из камня, а позже из металлов, посуду изготовлял из глины, одевался в шкуры животных, силой ветра приводил в движение парусные корабли и мельничные жернова. Каждый день люди наблюдали за явлениями природы, стремясь разгадать её тайны. А природа ещё тот Великий Химик! Секреты свои сразу не открывала. Человек не сразу получал ответы на свои вопросы. Вот по-вашему, что такое костёр? Оказывается, в нём тайна скрыта. Люди заметили, что под действием огня одни вещества (и сама жизнь) исчезают, а другие вещества изменяют свои свойства. Например, обожженная сырая глина приобретает прочность. Люди использовали это, и так родилось гончарное дело. А потом научились выплавлять металлы из руд, а сплавляя металлы получать различные сплавы. Так появилась металлургия. Как интересно! Самый главный химик – это Природа, а первой Химической Лабораторией был Костёр! Николай Александрович Фигуровский, советский историк химии так его назвал. А первыми химическими реакциями, осуществлёнными человеком, были превращения веществ под действием огня.
Рассказ 2 (Химия в художественной литературе)
«Не так давно я прочитал роман Е. Войскунского и И. Лукодьянова «Ур сын Шама». Хочу зачитать вам отрывок из него: «Хижина искусника стояла на краю селения, возле густого кустарника, что рос вдоль берега большого канала. Тут было много хорошей глины, и искусник лепил кувшины и делал на них узоры и обжигал их в очаге. Тоже из обожженной глины делал он серпы для жатвы ячменя и остро их оттачивал. Ещё он умел плавить и ковать медь и делать из неё браслеты и украшения. Но самое большое умение искусника было такое. Он ставил на землю в два ряда множество горшков и наполнял их оцетом, который получается из скисшего винограда. Затем опускал в эти горшки медные пластинки и рыжеватые камни, которые он один умел находить. Потом связывал пластинки и камни тонкими верёвками, тоже медными, и вдруг между двумя кончиками медных верёвок проскользнула молния. Вскоре искусник вынул из горшка медный браслет, и браслет теперь был блестящий, не медный, а золотой». Что произошло с браслетами?»
Голоса из зала, рассуждают: Получается, что браслет покрылся слоем золота! Как же это возможно? А мы изучали на уроках процесс, который называется электролиз. И учитель нам рассказывал, что процесс электролиза применяют для осаждения металлов на поверхности металлических и неметаллических изделий.
Да, вы правы. Есть отрасль прикладной электрохимии, которая называется гальванотехника. Гальванотехника – это осаждение металлов на поверхности металлических и неметаллических изделий при помощи электролиза. Гальванотехника делится на гальваностегию и гальванопластику. А явление, которое описывается в отрывке называется гальваностегия, т. е. электролитическое осаждение тонкого слоя металла на поверхности какого-либо металлического предмета, детали. В результате предмет или деталь приобретает красивый вид. Сейчас мы знаем, что гальваностегию используют не только чтобы придать предмету красивый вид, её используют для защиты металлов от коррозии, предупреждения износа различных механизмов. Предлагаю посмотреть, как происходит процесс гальваностегии». Демонстрируется видео-опыт (слайд 3).
Рассказ 3 (становление химии как науки)
«Чтобы химия стала наукой, потребовались тысячелетия. Это было время различных открытий, укрепления теоретического фундамента, заключение союзов с другими естественными науками. Называть химию наукой впервые стал Михаил Васильевич Ломоносов – величайший новатор в истории химии всех времен. Он по-новому осознал роль и значение химии, ее место среди наук, изучающих природу. Для Ломоносова химия – «наука изменений» – учение о процессах, происходящих в телах. И мы на уроках говорили, что химия – наука о веществах и их взаимопревращениях. О пользе химии М. В. Ломоносов говорил в публичном собрании Императорской Академии Наук сентября 6 дня 1751 года:
«… Широко распростирает химия руки свои в дела человеческие, слушатели! Куда ни посмотрим, куда ни оглянемся, везде обращаются пред очами нашими успехи ее прилежания. В первые времена от сложения мира принудили человека зной и стужа покрывать свое тело; тогда по первом листвия и кож употреблении домыслился он из волны и из других мягких материй приготовлять себе одежды, которые хотя к защищению телa его довольно служили, однако скучливое одним видом человеческое сердце и непостоянная охота требовали перемены; гнушались простою белизною и, пестреющим полям завидуя, подобного великолепия и в прикрытии тела искали. Тогда химия, выжимая из трав и из цветов соки, вываривая коренье, растворяя минералы, и разными образы их между собою соединяя, желание человеческое исполнять старалась и тем сколько нас украсила, не требуете слов моих к доказательству, но очами вашими завсегда ясно видите».
Получается, что всё материальное содержание человеческой цивилизации состоит сегодня так или иначе из продуктов химической промышленности. И в самом деле…. Химия изменила быт человека. Без достижений химии не было бы фотографии, кино, телевидения. Сегодня именно химики помогают агрономам и животноводам, чтобы у человека были продукты питания, придумывают способы получения различных тканей, создают конструкционные материалы для автомобилестроения, а также для самолёто- ракетостроения. Также химии принадлежит почётное место среди наук, подготовивших возможность межпланетных путешествий».
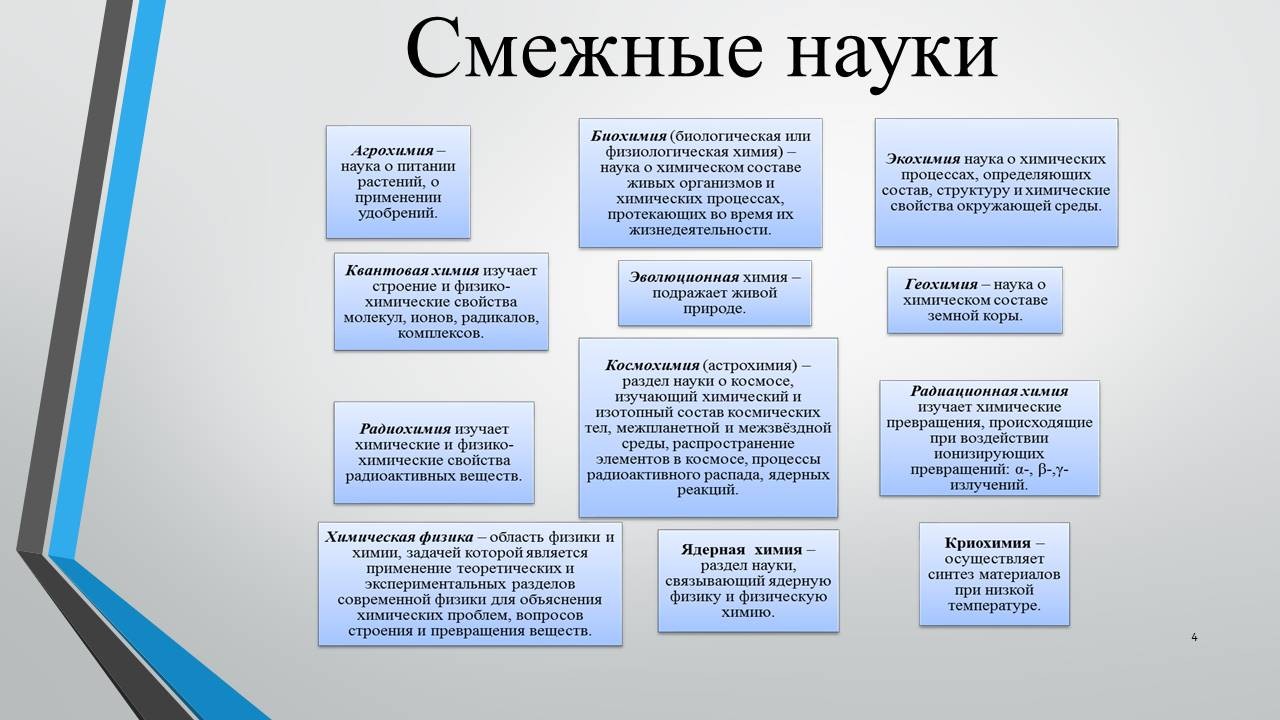
Рассказ 4 (интеграция химии с другими науками)
«Думается, что одной химии с таким обширным полем деятельности совершенно не справиться. И она заключает союзы с другими естественными науками. И с физикой подружилась, и с математикой. Как не вспомнить М. В. Ломоносова, который сказал, что «химия – правая рука физики, математика – ее глаз», а также «стремящийся к ближайшему изучению химии должен быть сведущ и в математике». Обратите внимание, на другие дружественные союзы». (Все рассуждают о смежных науках), (слайд 4).
Второй ведущий: Есть ещё желающие рассказать нам что-нибудь о науке химии?
Голоса из зала: Мы можем!
Первый ведущий: Выходите на сцену.Мы все слушаем.
Участники поочерёдно выходят на сцену и начинают рассказывать:
Рассказ 5 (химия и нанотехнологии)
«Наука развивается и идёт вперёд. Идёт очень быстро! «Через тернии к звёздам!» Так можно сказать, о новой области исследований не только химиков, но и физиков. Мы даже не задумываемся о том, что окружающий нас мир наполнен разнообразными биологическими нанообъектами и наноэффектами, о нанометрической сущности которых мы и не подозревали. Это, например, вирусы, аминокислоты, гемоглобин, бактерии. Сегодня химики и физики научились получать различные наноматериалы, их используют в различных сферах нашей жизни. В медицине с помощью нанотехнологий можно разрабатывать новые лекарства и медицинскую технику, используя нанопрепараты в сельском хозяйстве можно увеличить урожайности культур. Ещё есть интересное направление – военные нанотехнологии. Здесь исследуют энергетические ресурсы и боеприпасы, защитные и самовосстанавливающиеся системы, позволяющие автоматически ремонтировать повреждённую поверхность танка или самолёта, или менять её цвет (эффект хамелеона), устройства обнаружения химических и биологических загрязнений».
Рассказ 6 (химическая экология)
«Есть ещё наука, которая образовала союз с химией – химическая экология. Эдуард Григорьевич Раков, профессор кафедры нанотехнологии и наноматериалов Российского химико-технологического университета им. Д. И. Менделеева, член Водородного клуба Московского государственного института радиотехники, электроники и автоматики, говорит об этой науке так: «Химическая экология – раздел экологии, науки об основах рационального природопользования и охраны окружающей среды. Она изучает разнообразные химические процессы в окружающей среде, естественные кругообороты веществ и влияние на них деятельности человека, химические методы и средства защиты окружающей среды. Именно человечество превратилось в основного нарушителя природных равновесий. О масштабах химических изменений говорят такие примеры. Ежегодные выбросы углекислого газа составляют сейчас примерно 200 млрд т. Эта величина превышает способность Мирового океана к его поглощению (океан поглощает СО2 довольно медленно), что вызывает увеличение концентрации СО2 в атмосфере Земли и постепенное потепление климата на планете. Парниковый эффект, предсказанный учеными, сейчас проявляется весьма наглядно. Широкое применение фреонов – хладонов привело к появлению «озоновых дыр», т. е. к утончению озонового слоя атмосферы, и повышению риска получить заболевания кожи. До определенного времени природе удавалось залечивать свои раны, включать выбрасываемые промышленные отходы в естественные циклы, уничтожать эти отходы. Наконец пришло понимание, которое хорошо выразил поэт Василий Федоров:
Земли не вечна благодать.
Когда далекого потомка
Ты пустишь по миру с котомкой,
Ей будет нечего подать.
Примерно в 1960–1970-е годы различным разделам экологии стало уделяться все большее внимание, экологические проблемы стали решаться на государственном, а некоторые – и на международном уровне. Сегодня к достижениям химической экологии относится разработка каталитического дожигания выхлопных газов автомобилей, плазменных процессов уничтожения особо токсичных отходов, биохимических методов обезвреживания сточных вод. Особенно важное значение имеют химические методы в обеспечении безопасности ядерной энергетики, в частности при обезвреживании высокорадиоактивных отходов. Химические методы могут сыграть решающую роль в замене традиционной угольной энергетики – одного из основных загрязнителей воздуха – экологически более чистыми способами производства энергии. Разрабатываются, в частности, методы превращения угля в жидкое органическое топливо (это снизит потери при перевозке угля и главное – устранит громадные выбросы вредных веществ при его сжигании). Принципиально новым этапом в развитии экологически чистой промышленности и энергетики станет водородная энергетика, которая предполагает использовать водород в качестве энергоносителя».
Первый ведущий: Рассказы о химии очень познавательны! Но вот, читая очень старый журнал, я нашёл странные записи. Посмотрите на экран. Как вы думаете, что они означают? (слайд 5)
Голоса из зала, рассуждают: Что-то не совсем понятно. На химические формулы непохоже. Очень необычные записи. Тайнопись какая-то!
Второй ведущий: И не просто тайнопись, а, внимание на экран. (На экране появляется текст). «Химическая тайнопись!». (слайд 6) Кто-нибудь может нас просветить, что же это за тайнопись?
Голос из зала: Я могу вам помочь.
Рассказ 1 об алхимических символах
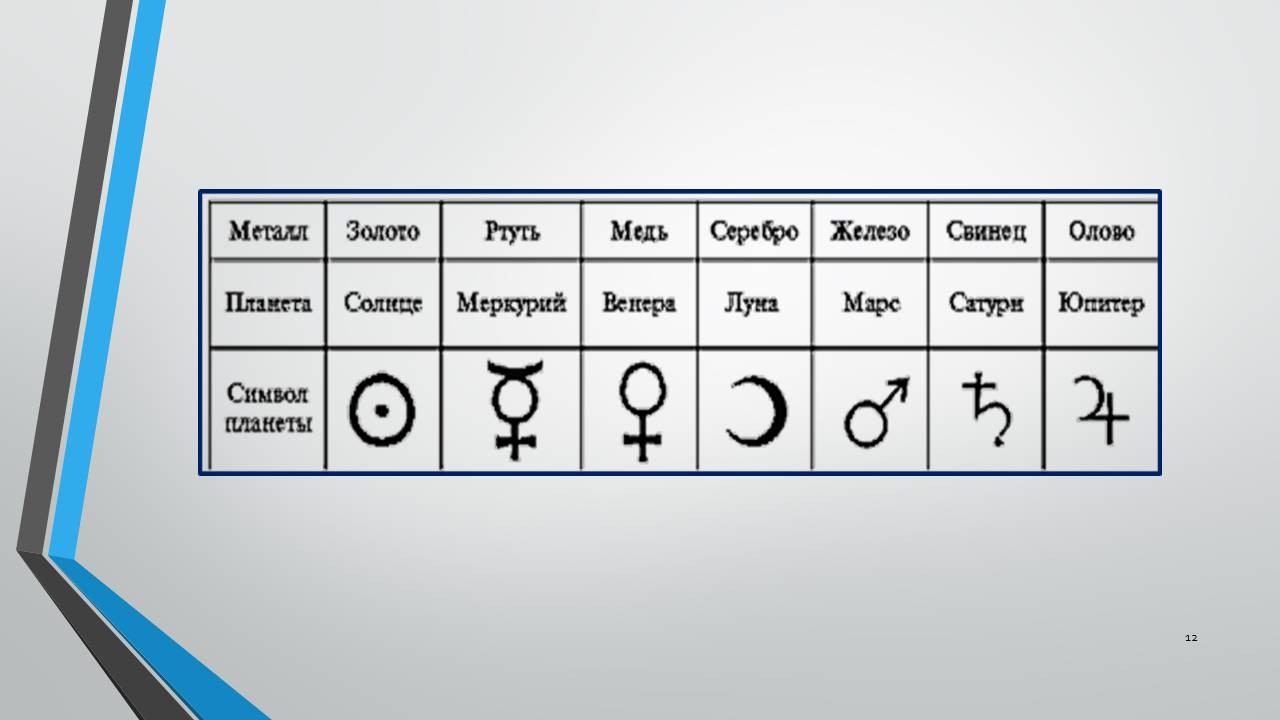
«Впервые термин «алхимия» встречается в «Учение в восьми книгах» Юлия Фирмика Матерна, латинского писателя и астролога IV века (слайд 7). Родиной алхимии считается Древний Египет. Родившаяся в Александрии алхимия сразу же обзавелась небесным покровителем – им стал египетский бог Тот (Джехути) – бог луны, мудрости, счета и письма, покровитель наук, писцов, священных книг, создатель календаря (слайд 8). Арабский книжник 10 века Ибн аль – Надим (слайд 9) полагал, что родоначальником алхимии был Гермес Великий, родом из Вавилона, поселившийся в Египте после Вавилонского столпотворения. И на протяжении всего своего существования алхимия оставалась наукой герметической – закрытой для непосвящённых. Свои сосуды алхимики запечатывали печатью с изображением Гермеса (слайд 10)– отсюда выражение «герметически закрытый». Так, в Древнем Египте некоторые вещества изображали специальными иероглифами. Смотрите! (слайд 11). Основными объектами изучения александрийской алхимии являлись металлы. В то время было известно семь металлов. Это число соотносилось с числом известных тогда планет – Солнцем, Луной, Меркурием, Венерой, Марсом, Юпитером, Сатурном. Под влиянием лучей этих небесных светил, учили алхимики, в недрах Земли зарождаются и совершенствуются металлы. Каждая планета имела свой особый знак, который одновременно служил и символом металла, находящегося под её влиянием. Вот эти знаки (слайд 12):

Об этих металлах алхимики сочинили стихи, слушайте!
«Семь металлов создал свет
по числу семи планет.
Дал нам космос на добро:
медь, железо, серебро,
злато, олово, свинец,
сын мой, сера – их отец.
И спеши, мой сын, узнать:
всем им ртуть – родная мать».
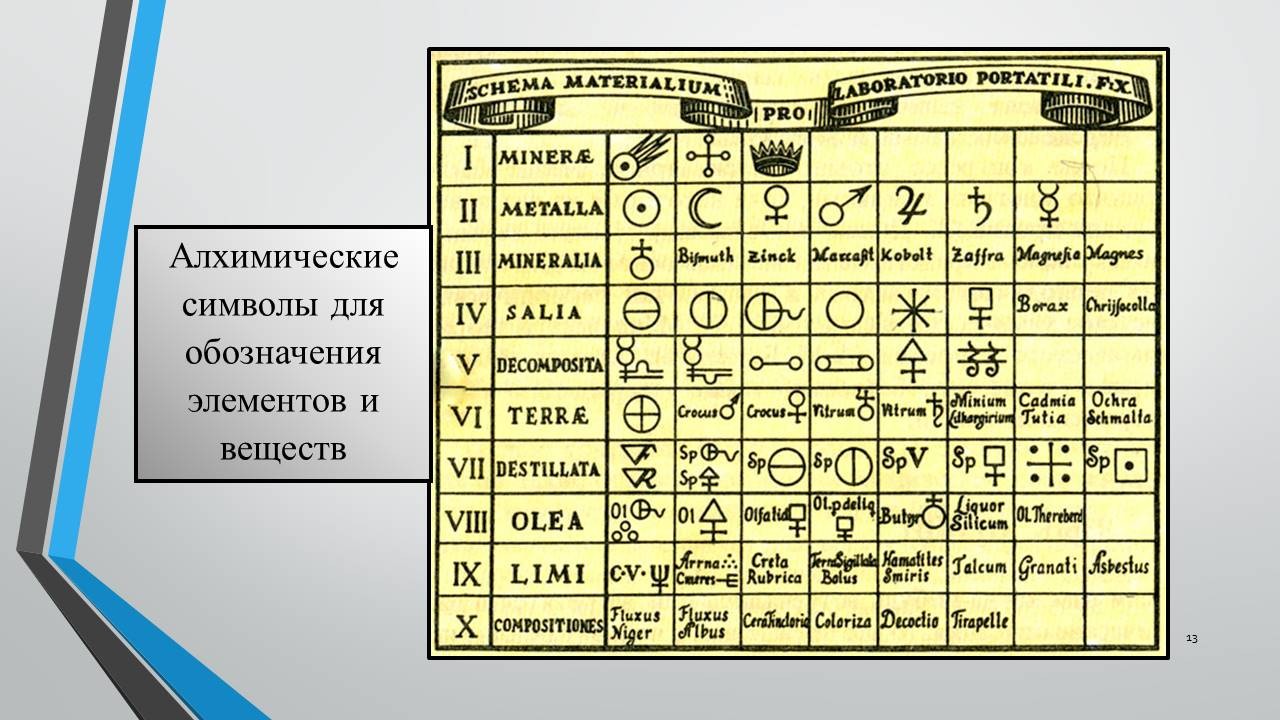
Существовало предание, что искусству обращать простые металлы в золото ангелы научили земных женщин, с которыми вступили в брак, о чем рассказано в «Книге Бытия» и «Книге пророка Еноха» в Библии. Это искусство было изложено в книге, которая называлась «Хема». Алхимики стремились придать изображениям химических веществ таинственный смысл, зашифровать их при помощи символов. Химические знаки алхимиков имели самые причудливые фигуры. Смотрите! (слайд 13). Алхимики изображали символами не только элементы, но и вещества, а названия-то у веществ какие!
«Серый Волк» – так обозначалась металлическая сурьма в работе с минералами, так как, будучи расплавленной, она жадно поглощала многие другие металлы, такие как медь, олово и свинец, образуя сплавы.
«Зелёный Лев» – зеленым львом обычно именовался Vitriolum или серная кислота, получаемая путем дистилляции в сосуде зеленых кристаллов сульфата железа, Зеленый Лев также мог бы быть азотной кислотой, получаемой путем нагревания селитры и сульфата железа. Для тех же алхимиков, что работали главным образом с растительной материей, Зеленый Лев пожирающий солнце – это зеленый пигмент хлорофилл.
«Красный лев» – киноварь, сурьмяная киноварь, колькотар – коричневая минеральная краска, свинцовый глет, сурик.
В своих аллегориях алхимики часто использовали также человеческие, животные и растительные эмблемы, иногда причудливые сочетания фигур – такие, как дракон – так называли и селитру, и сулему, и огонь, все с чего начинались опыты, дракон чаще бывает связанный с Меркурием – ртутью, единорог – в алхимии его символ значил духовную эволюцию, рог описывается как символ проникновения духа в материю, символ силы волшебников и магов и феникс – символ философского камня (слайд 14).
К началу XVIII века в алхимии насчитывалось около 4000 символов и пользоваться ими становилось всё труднее. Все алхимические символы были разработаны с одной основной целью: скрыть от непосвящённых людей тайную информацию, касающуюся алхимических опытов. Алхимическими знаками выражали качественный состав молекул и в химии XVIII века (слайд 15).
(все участники вечера изучают представленную информацию)
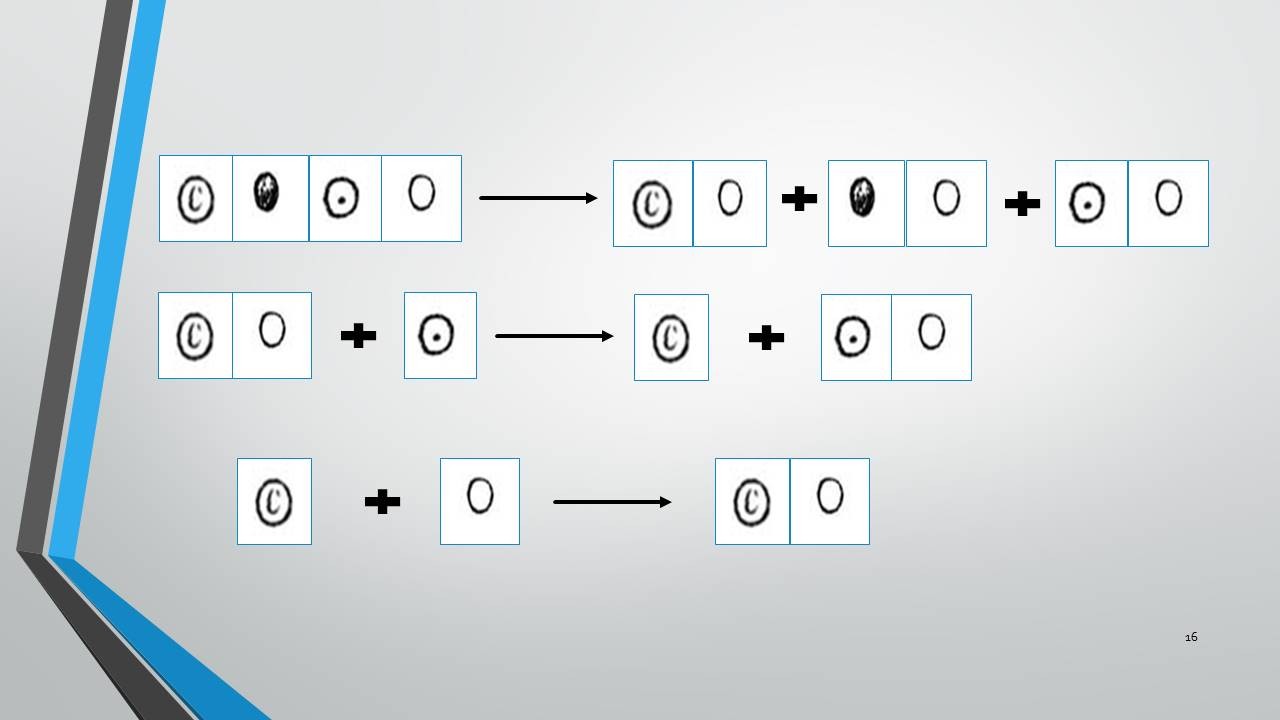
Первый ведущий: Итак, с вашей помощью нам удалось расшифровать одну из таинственных записей. А я в одной очень старой книге нашёл ещё более загадочную и ещё более интересную запись. Смотрим (слайд 16). Что-нибудь эта необычная запись вам говорит?
Голоса из зала: Вообще какая-то абракадабра.
Второй ведущий: Неужели никто нам не поможет. Есть у кого-нибудь какие-то мысли?
Голос из зала: Я могу вам помочь разобраться с этой абракадаброй.
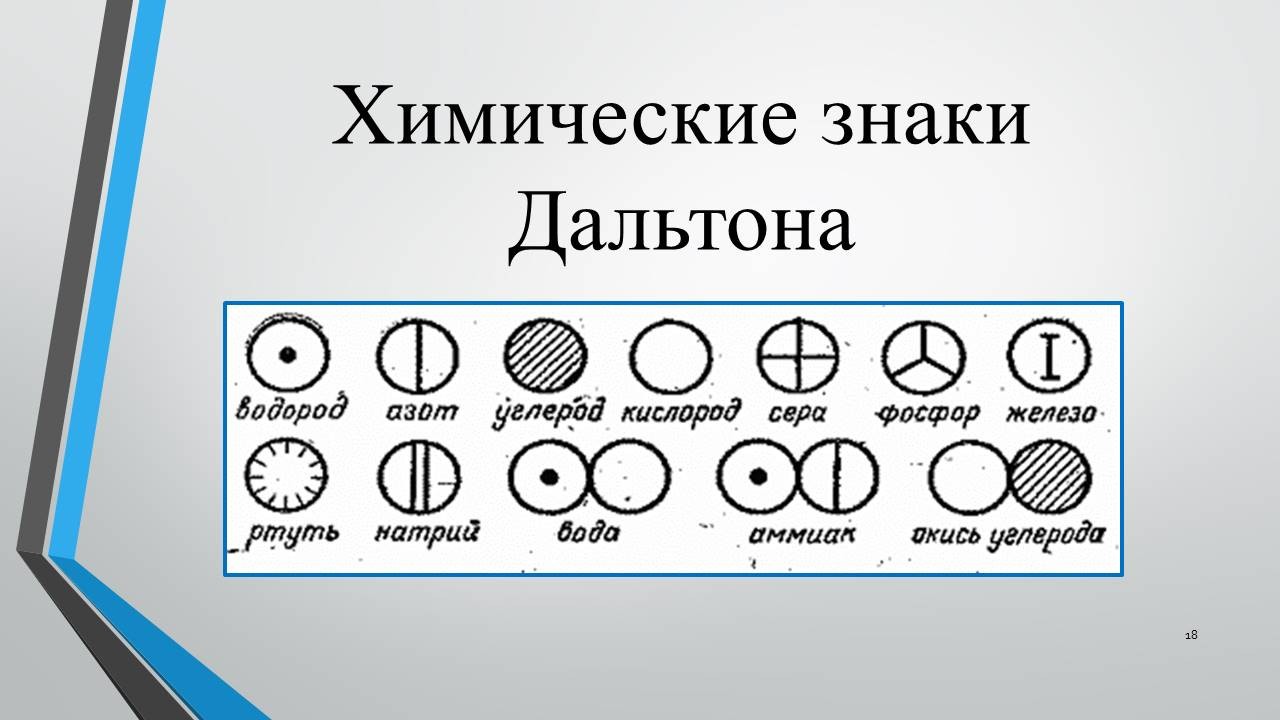
Рассказ 2 о символике Д.Дальтона
«Английский провинциальный учитель-самоучка, химик, метеоролог и естествоиспытатель Джон Дальтон вводит новую химическую символику – обозначает химические элементы кружками с точками, черточками или буквами внутри. Это был 1803 г. Изображая молекулы веществ, Дальтон указывал не только из каких элементов состоит вещество, но и сколько атомов каждого элемента в молекуле. Смотрим! (слайд 17)

Таким образом, предложенные Дальтоном формулы отражали не только качественный состав соединений, но и количественный» (слайд 18, 19).
(все участники вечера изучают представленную информацию)
Первый ведущий: Но в настоящее время мы используем современную символику. Как она возникла? Кто может рассказать?
Голос из зала: Я могу вам рассказать.
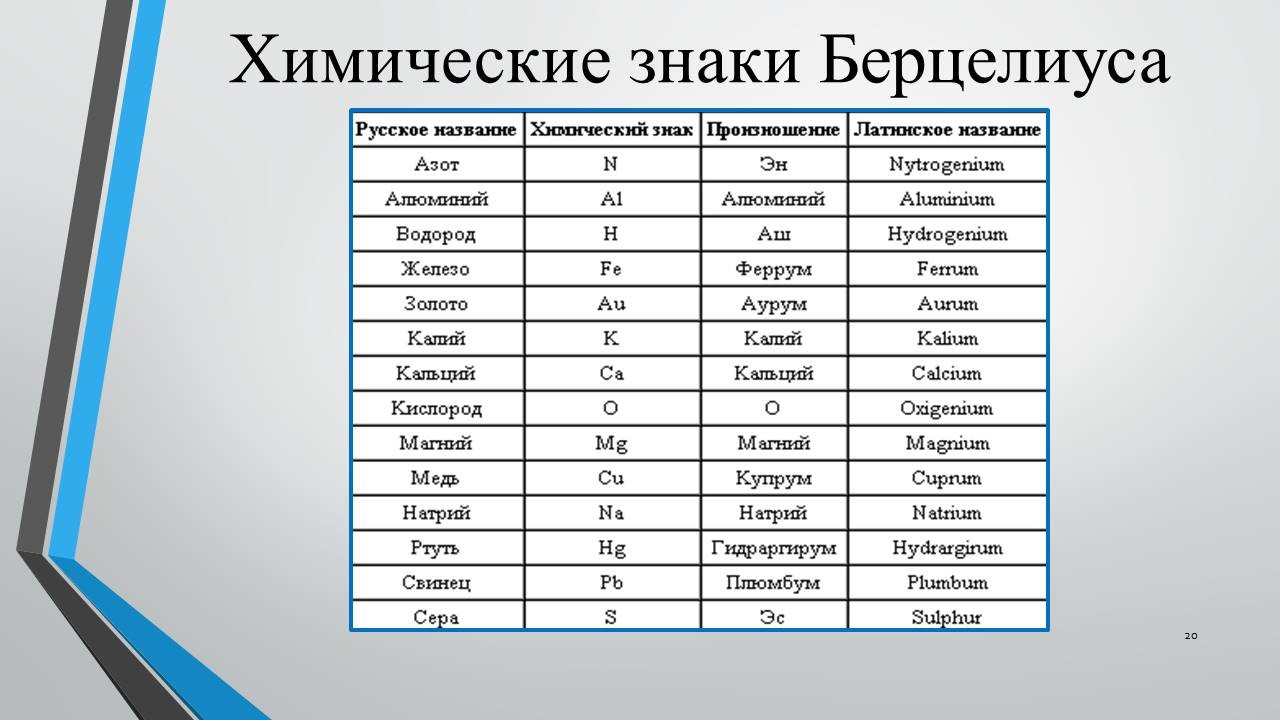
Рассказ 3 о символах Й.Я. Берцелиуса
«Символы Дальтона были значительно проще алхимических, но все же очень неудобны для печати. Об этом говорил Берцелиус. В 1813 г. он опубликовал свою систему химических символов, а в следующем году вышла его работа «О причине химических пропорций и о некоторых сюда относящихся вопросах вместе с простым способом изображения последних». «Химические знаки должны быть буквами», - считал Берцелиус, - чтобы объяснить написанное, а не портить книгу». Он решил обозначать химические знаки элементов начальными буквами их латинских названий. Например, сера по-латыни sulfur и обозначается S; олово – stannum, обозначается Sn; сурьма – stibium, обозначается Sb и т. д. Если первая буква в названии элементов была одинакова, Берцелиус отличии от своих предшественников забирал из названия две буквы. Так возникли современные обозначения химических элементов. Ученые по достоинству оценили нововведение Берцелиуса, новые знаки довольно быстро и прочно вошли в химию. Но были у системы Берцелиуса и противники, самым непримиримым среди которых был … Дальтон. Он называл новые химические формулы «хаосом атомов». Однако этими символами мы пользуемся по сей день. С введением буквенных символов стало легко записывать химические формулы. Число атомов в молекуле Берцелиус обозначал цифрой, которую сначала ставил слева от знака элемента. В 1834 г. знаменитый немецкий химик Юстус Либих предложил обозначать число атомов элемента в молекуле подстрочным цифровым индексом, помещая его справа внизу от символа элемента. Формулы химических соединений приняли привычный для нас вид. Несмотря на широкое распространение новых символов в мире, в России они привились не сразу. Только в 1824 г. в «Новом магазине естественной истории, физики, химии и сведений экономических» была опубликована статья врача и популяризатора медицинских знаний И. Я. Зацепина «О берцелиевых законах химического сродства», в которой приводились символы химических элементов, их атомные веса и формулы некоторых соединений» (слайд 20).
Второй ведущий: Да, путь к современному химическому языку оказался очень тернист. Современную химическую символику можно назвать своеобразным алфавитом. С его помощью записывают слова, то есть формулы соединений и фразы, то есть уравнения химических реакций. А химические реакции в той или иной мере отражают реально происходящие процессы. Кстати, химические уравнения в России первым стал применять знаменитый ученый Герман Иванович Гесс, открывший закон постоянства количества теплоты реакции. В учебнике «Основания чистой химии» (1831-1833) он приводит формулы и уравнения реакций не только неорганических, но и органических веществ.
Первый ведущий: Вот я и предлагаю, используя современный химический язык, показать, что же было написано с помощью алхимических знаков и знаков Д. Дальтона.
(Показывается слайд 5, а на переносной доске участники пишут уравнения).
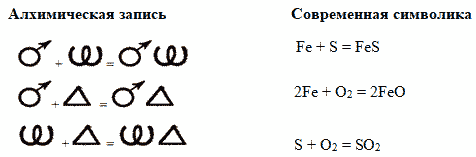
Голоса из зала: Алхимическая запись не точная. С помощью алхимических знаков нельзя записать точную формулу вещества.
Второй ведущий: Вы очень наблюдательны. Переведём на современный химический язык запись с помощью символов Д.Дальтона.
(Показывается слайд 16, а на переносной доске участники пишут уравнения).
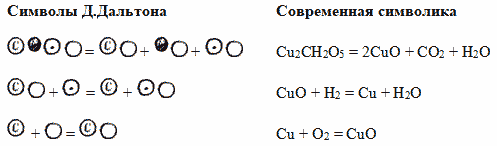
Голоса из зала: Символика Берцелиуса очень удобна и понятна.
Первый ведущий: Русский хирург и анатом, естествоиспытатель и педагог, создатель первого атласа топографической анатомии, основоположник русской военно-полевой хирургии, основатель русской школы анестезии Николай Иванович Пирогов сказал: «Учитесь, читайте, размышляйте и извлекайте из всего самое полезное». И вы все присутствующие, последовали этому совету – размышляя, вы сделали вышесказанные выводы о языке химии.
Второй ведущий: Из ваших высказываний можно сделать вывод, что у химии, равно как и у любой другой науки, есть свой язык! Вы согласны? (обращается к зрителям).
Голоса из зала: Да, конечно, согласны. Например, математика разговаривает с помощью цифр, а у русского языка – это буквы, из которых складываются слова. У литературы – это слова, которые можно сложить в красивые выражения, а словами можно выразить свои мысли!
Первый ведущий: Так выскажите свои мысли! Как вы думаете – связаны ли друг с другом химия и русский язык?
Голоса из зала: Конечно, на уроках химии мы говорим на русском языке, но специфический химический язык, т.е. язык формул мы также используем. И на языке формул на уроках химии общаться интереснее.
Второй ведущий: Вот мы говорим, что у каждой науки есть свой язык, а оказывается есть специальная наука. Она называется лингвистика. Это наука о языке в целом как об основном средстве общения между людьми. Задача лингвиста — не столько выучить язык, сколько объяснить принципы его устройства, выявить, каким образом его особенности – произношение, грамматика, алфавит – влияют на людей и общество, которые на нем говорят.
Первый ведущий: Кто-нибудь может сказать имеет ли отношение к химии лингвистика?
Голоса из зала: На уроках химии вначале мы изучаем знаки элементов, их произношение, учимся составлять формулы различных веществ, писать уравнения реакций, отмечаем признаки происходящих явлений. И чтобы в совершенстве знать химический язык, также изучаем законы химии.
Ведущие (вместе): Вы хотите сказать, что задачи лингвиста и задачи химика практически совпадают?
Голоса из зала: Да! Совершенно верно!
Ведущие (вместе): А знаете ли вы, как решают поставленные задачи химики? Какие способы и методы используют?
Голоса из зала: Химики используют наблюдение, эксперимент, моделирование.
Второй ведущий: Представьте себе, лингвистика может решать свои задачи используя методы наблюдения, экспериментирования, формулировки гипотез, интерпретации. Не находите ничего общего?
Голоса из зала: Химия заключила союз с физикой, биологией, геологией, механикой. Химия подружилась даже с электроникой. А может ли химия подружиться с лингвистикой? Ведь даже методы обе науки используют одинаковые? Что скажете, уважаемые ведущие?
Первый ведущий: Посмотрите на экран. (слайд 21) (Появляется текст) «Химическая … лингвистика!». И это очередное наше открытие. Из двух наук – химии и лингвистики образовалась химическая лингвистика. Предлагаем вам перевоплотиться в химических лингвистов и найти ответы на очень интересные вопросы.
Лингвистические упражнения (слайды 22-37); упражнения можно выполнять выборочно:
- Анаграмма – перестановка букв в словах с образованием нового слова.
Примеры:
- Из названия какого химического элемента, переставляя первую букву в конец слова, можно получить название полезного ископаемого?
(фтор – торф)
- Из названия какого химического элемента, переставляя первую букву в конец слова, можно получить название одного из видов четырехугольника?
(бром – ромб)
- Какой элемент при перестановке двух букв в его названии превратится в музыкальный инструмент?
(аргон – орган)
- Какой элемент, если отбросить первую букву в его названии, превращается в напиток, а если изменить одну букву, то превратится в церковь?
(хром – ром – храм)
- Какой элемент становится столярным инструментом, если в его названии заменить первую букву?
(золото – долото)
- Назовите душистое вещество, название которого без первой буквы превращается в основу многих красящих веществ.
(ванилин – анилин)
- Какой элемент при добавлении впереди одной буквы превращается в метель?
(уран – буран)
- Какой элемент после отбрасывания в его названии одной средней буквы и при чтении в обратном порядке превращается в кондитерское изделие?
(теллур – рулет)
- Название какого растворителя после отбрасывания первой буквы превращается в стихотворное произведение?
(вода – ода)
- Отбросив первую букву в названии органического вещества и прочитав полученное слово в обратном порядке, вы получите название подводной скалы. Назовите это вещество.
(эфир – риф)
- Назовите элемент, который при добавлении в его названии впереди одной буквы обозначает полупроводниковый прибор.
(йод – диод)
- Назовите углеводород, который, если отбросить в его названии первую букву и прочитать то, что осталось в обратном порядке, становится показателем движения воды в водопроводе.
(пропан – напор)
Примеры:
1. Переставив приведённые буквы, вы получите ряд, в котором можно прочитать названия двух элементов так, что конечные буквы названия первого элемента станут начальными буквами названия второго элемента.
а) РЕМОРБЕС
б) ЕСДОНРА
в) ИЙРОТФ
Ответ: а) серебро, бром; б) сера, радон; в) фтор, торий
2. Переставив приведённые буквы, вы получите ряд, в котором можно прочитать названия трёх элементов так, что конечные буквы названия первого элемента станут начальными буквами названия второго элемента, а конечные буквы названия второго элемента станут начальными буквами названия третьего элемента.
а) ИАТЛИЙЛАНТТ
б) ОООДРДИЙОДВПО
Ответ: а) тантал, талий, литий; б) водород, родий, олово.
3. Сколько названий химических элементов вы сможете составить из букв, входящих в предложения? (Одинаковые буквы можно использовать несколько раз, букву «и» можно заменить «й»).
а) Периодическая система элементов.
б) Периодический закон Менделеева.
в) Теория строения атома Бора.
г) Теория электролитической диссоциации.
Ответ:
а) йод, платина, селен, титан, неодим, лантан;
б) радий, ванадий, родий, йод, селен;
в) бром, титан, бор, палладий, серебро, ниобий, барий, самарий;
г) литий, калий, церий, торий, таллий; (кто-то найдёт другие названия элементов).
Голоса из зала: Однажды на уроке наш учитель прочитал нам рассказ-загадку о воде. А нам о «горючем воздухе». И нам тоже учитель читал об «оловянной чуме» и о загадке серебряных бокалов. Было очень интересно.
Второй ведущий: И ведь это же опять открытие! Вроде бы химия, сплошные формулы, уравнения и вдруг – рассказы! Да не просто рассказы, а загадки! Как тут не удивляться?! Смотрим на экран. (слайд 38) (Появляется текст) «Химические поучительные рассказы-загадки».
Голоса из зала: Мы можем рассказать всем рассказ-загадку «Оловянная чума» и показать видео-опыт.
Первый ведущий: Слушаем рассказ-загадку «Оловянная чума».
Рассказ-загадка «Оловянная чума»
«Руки интенданта, открывавшего склад, заметно дрожали: внезапный приезд ревизора ничего хорошего ему не сулили. Однако лицо его продолжало сохранять выражение величайшей почтительности и готовности немедленно выполнить любое приказание высокого начальства.
- Здесь у нас хранятся оловянные пуговицы для солдатских мундиров, - доложил он, распахивая двери склада.
- Посмотрим, как они у вас хранятся, - буркнул в ответ старший ревизор. – Откройте! – кивнул он, указывая в сторону одного из больших деревянных ящиков.
С тем же выражением почтительности на лице интендант подлетел к ящику, рывком поднял его крышку и … остолбенел от неожиданности и удивления: ящик был доверху наполнен, но не блестящими оловянными пуговицами с двухглавым орлом, а каким-то сероватым порошком.
- И в других ящиках у вас такие же «пуговицы»? – ехидно спросил старший ревизор.
К ужасу интенданта таким же порошком оказались заполнены все без исключения ящики.
- Ну-с, милостивый государь! – обратился к нему старший ревизор после осмотра последнего ящика. – Что вы теперь скажете нам? Куда дели доверенные вам пуговицы?
Несмотря на страшный холод в складе интенданту стало жарко.
- Ничего не понимаю, ваше превосходительство! – пролепетал он в ответ. – Все они должны находиться в этих ящиках!
- Вы, кажется, за дурака принимаете меня, милостивый государь! – закричал ревизор. – В таком случае, - обратился он к одному из своих помощников, - возьмите немного этого вещества и отправьте его в нашу лабораторию. Химики точно скажут, что именно он положил в ящики вместо украденных пуговиц, и помогут нам запрятать этого вора подальше в Сибирь!
Через несколько дней удивляться пришлось и ревизорам: «Присланное вами для анализа порошкообразное вещество, - писал в своём заключении начальник лаборатории, - несомненно, олово. Очевидно, в данном случае имело место явление, известное в химии под названием «оловянная чума».
Второй ведущий: Что же произошло с оловянными пуговицами, и почему именно это явление называется «оловянной чумой?
Голос из зала: Я могу объяснить.
На сцену выходит участник и объясняет этот рассказ-загадку. Показывает видео-опыт, (слайд 39).
Ответ на вопросы рассказа-загадки «Оловянная чума».
При низких температурах белое олово распадается в порошок, превращаясь в другое аллотропное видоизменение олова – «серое олово». Превращение медленно распространяется вокруг от той точки, где оно началось. Этот процесс очень напоминает распространение воспалительных процессов в живых организмах. Поэтому превращение белого олова в серое получило образное название «оловянная чума».
Голоса из зала: А мы можем загадать вам загадку о серебряных бокалах. Попробуйте её отгадать.
Первый ведущий: Хорошо, слушаем загадку о серебряных бокалах.
Рассказ-загадка о серебряных бокалах
«Весной 327 года до нашей эры знаменитый греческий полководец Александр Македонский вторгся в пределы Индии (слайд 40). Однако здесь он встретил не только мужественное сопротивление свободолюбивого народа, но и другого страшного врага – кишечные заболевания.
До крайности уставшие и изнурённые болезнями солдаты не выдержали, взбунтовались и принудили отдать приказ о возвращении домой.
Как видно из оставленного историками описания этого похода, военачальники армии Александра Македонского заболевали значительно реже, чем рядовые воины, хотя вместе с ними переносили невзгоды походной жизни и пили одну и ту же воду.
Причина этого загадочного явления была найдена лишь спустя 2250 лет. Она состояла в том, что рядовые воины греческой армии в то время пользовались в походах оловянными бокалами, а военачальники – серебряными».
Второй ведущий: Кто может объяснить, почему, пользуясь серебряными бокалами, военачальники армии Александра Македонского были менее подвержены кишечным заболеваниям в этом походе?
Голос из зала: Я могу объяснить.
На сцену выходит участник и объясняет этот рассказ-загадку, показывает видео-опыт, (слайд 41).
Ответ на вопросы рассказа-загадки «О серебряных бокалах».
Как и все вещества, серебро хотя и мало, но растворяется в воде. Растворённое в воде серебро обладает замечательным свойством – убивает находящиеся в воде болезнетворные бактерии. (Чтобы полностью обеззаразить один литр воды, достаточно нескольких миллиардных долей грамма серебра). Так как военачальники армии Александра Македонского пользовались серебряными бокалами, это в какой-то мере предохраняло их от заболеваний, вызывавшихся микробами, находящимися в воде, которую им приходилось пить так же, как и рядовым воинам.
Голос из зала: А знаете ли вы, что такое «сухой лёд»? Хотите послушать?
Первый ведущий, обращаясь к участникам: Будем слушать?
Голоса из зала: Конечно, мы слушаем.
Рассказ-загадка «Сухой лёд»
«Когда Вася Петушков подошёл к продавщице мороженного, она высыпала в коробку со своим товаром кусочки какого-то вещества, похожего на снег.
- Подожди немного, мальчик, - попросила она, - пока я добавлю к мороженому «сухого льда».
- За кого вы меня принимаете? – возмутился Вася. – Я в восьмом классе учусь, по физике и по химии у меня пятёрки. Лёд – это замёрзшая вода и не может быть сухим так же, как и горячим!
- Вот как?! – удивилась девушка и, подавая ему кусочек льда, сказала: - А ну, докажи, что он не сухой!
Перебрасывая с одной ладони на другую обжигающий холодом кусочек льда, Вася всё больше удивлялся: он быстро таял, не оставляя даже признаков влаги.
- Что же это такое, в самом деле?! – думал он, чувствуя, как лицо и уши его загораются от стыда за понесённое поражение.
- Теперь, знаток физики и химии, - сказала девушка, протягивая ему брикет мороженого, - скажу тебе по секрету, что лёд может быть не только сухим, но и горячим».
Второй ведущий: Что же представлял собой «сухой лёд» и действительно ли лёд может быть горячим?
На сцену выходит участник и объясняет этот рассказ-загадку, показывает видео-опыт, (слайд 42).
Ответ на вопросы рассказа-загадки «Сухой лёд».
При охлаждении до 80˚С или при сжатии до 60-70 атм. углекислый газ превращается в твёрдое вещество, похожее по внешнему виду на лёд. В отличии от обыкновенного льда «сухой лёд» не тает, а испаряется, переходя сразу из твёрдого состояния в газообразное, за что и получил своё название. Испарение его сопровождается поглощением большого количества тепла: при испарении 1 килограмма «сухого льда» поглощается до 150 ккал тепла, то есть в два раза больше, чем при таянии 1 килограмма обыкновенного льда. При нормальном давлении обыкновенный лёд тает при нуле градусов. При высоких давлениях точка плавления его сильно повышается, при давлении в 10000 атм., например, он плавится лишь при температуре выше 50˚С, то есть действительно может быть и горячим.
Первый ведущий:
Свойства веществ – самые различные нужно знать!
Чтобы явления с ними происходящие, уметь объяснять!
А также поучительные, весёлые, интересные
рассказы и сказки химические сочинять!
Второй ведущий: Как сказал советский физик, видный организатор науки Пётр Капица «Наука должна быть весёлая, увлекательная, простая». А химия к тому же ещё и экспериментальная! В своём «Слове о пользе химии, в публичном собрании Императорской Академии Наук сентября 6 дня 1751 года говоренное», М. В. Ломоносов сказал: «Химик требуется не такой, который только из одного чтения книг понял сию науку, но который собственным искусством в ней прилежно упражнялся; … который великое множество опытов делал …». Д. И. Менделеев в опыте усматривал средство «вопрошать природу и получать от неё ответы в лабораториях». Он писал: «Опыт есть посредник между явлениями природы и познавательными способностями».
Первый ведущий:
Есть опыты научные, серьёзные;
есть опыты простые и сложные.
А в занимательной и весёлой химии
есть опыты интересные и красивые.
А есть весёлые и эффектные!
Мы сделаем их своими руками!
Итак, друзья, химическая «магия», ура!
Появляется надпись (слайд 43) «Весёлая и занимательная химия».
Второй ведущий: Вы уже догадались, что сейчас будут опыты, и не просто опыты, а опыты-загадки.
Опыты проделывают подготовленные учащиеся под руководством учителя.
Опыты-загадки
«Огонь-художник»
На большом листе бумаги (ватмана) концентрированным раствором калиевой селитры (нитрата калия) нарисовать большой цветок и написать «О, химия!» Рисунок и надпись нужно делать одной непрерывной линией без пересечений. От контура рисунка тем же раствором необходимо провести линию к краю бумаги, отметить конец линии карандашом. Дать рисунку высохнуть, рисунок станет невидимым. Затем тлеющей лучинкой прикоснуться к карандашной метке, огонёк, передвигаясь по контуру рисунка «проявит» его.
Объяснение опыта: Калиевая селитра или нитрат калия легко разлагается при нагревании, при этом выделяется кислород. Кислород поддерживает горение, поэтому бумага по линиям рисунка будет медленно сгорать, «проявляя» рисунок.
«Фараонова змея»
На кирпич установить тарелку. В неё насыпать конусом песок, пропитанный спиртом. В верхней части конуса сделать углубление, положить в него смесь 2 граммов питьевой соды, 13 граммов сахарной пудры, хорошо растёртых в ступке. Поджечь спирт. Через некоторое время из конуса появится чёрная «змея», которая извиваясь, выползает через край тарелки и падает на подставку.
Объяснение опыта: При нагревании сахар плавится и обугливается, а из соды выделяется углекислый газ, который и заставляет ползти «змею». Чем дольше горит спирт, тем длиннее получается «змея».
«Свинцовая шуба»
Из цинковой пластинки вырезать фигурку человека. Приготовить раствор ацетата свинца, для этого в 100 мл горячей воды растворить 20 граммов ацетата свинца. Фигурка покроется пушистым слоем кристаллов свинца, напоминающим меховую одежду.
«Сатурново дерево»
А если в раствор ацетата свинца опустить несколько связанных полосок цинка, то получится «Сатурново дерево».
Объяснение опытов: Происходит реакция замещения. Более активный металл (цинк) вытесняет из раствора менее активный (свинец).
«Магнитная капля»
На предметное стекло положить кристаллик хлорида железа (II). Кристаллик будет поглощать влагу из воздуха и быстро расползаться по стеклу, превращаясь в каплю. Каплю нужно поддеть распущенным концом толстой нити. Если поднести к ней магнит, то он притянет каплю.
Объяснение опыта: Раствор хлорида железа (II)обладает магнитными свойствами.
«Искусственные водоросли»
Шесть колб с плоским дном наполнить 50%-м раствором силиката натрия (жидкое стекло – Na2SiO3). В первую колбу бросить несколько кристалликов хлорида железа (FeCI2), во вторую – хлорида меди (CuCI2), в третью – хлорида кобальта (CoCI2), в четвёртую – хлорида никеля (NiCI2), в пятую – хлорида марганца (MnCI2), в шестую – хлорида алюминия (AICI3). Необходимо распределить кристаллики по всему объёму колб. Через некоторое время начинается рост «водорослей» причудливой формы и различной окраски.
Объяснение опыта: Брошенные в раствор силиката натрия кристаллики различных солей вступают с ним в реакцию. Образовались нерастворимые соединения - силикаты железа, меди, кобальта, никеля, марганца, алюминия. Они покрывают кристаллы исходных солей тонкой плёнкой, но тут начинается физика! В силу диффузии вода проникает сквозь тонкую плёнку, давление в кристаллах повышается, образовавшиеся хлориды металлов поглощают воду и «разбухают». А плёнка лопается. Через отверстия раствор солей проникает в окружающую жидкость и быстро вновь покрывается плёнкой. Затем плёнка опять прорывается. Так вырастают ветвящиеся, разноцветные «водоросли».
В растворе соли железа «водоросли» коричневого цвета, в соли меди – голубовато-зелёные, в соли кобальта – фиолетовые, в соли никеля – светло-зелёные, в соли марганца – розовые, в соли алюминия – бесцветные.
«Золотой дождь»
В одной колбе с кипящей водой растворить ацетат свинца, а в другой – иодид калия. Оба раствора слить в большую колбу, дать смеси остыть. Через некоторое время появляются красивые золотистые чешуйки, плавающие в растворе.
Объяснение опыта: Происходит реакция обмена в результате которой образуется осадок иодида свинца в виде жёлтых кристаллов.
«Секретные чернила»
На большом листе ватмана с помощью заострённой палочки написать раствором серной кислоты:
«О, химия, королева наук!
Ты учишь нас мудрости,
фантазировать позволяешь.
Весёлыми опытами природы
явления объясняешь».
Дать надписи высохнуть. Прогладить горячим утюгом лист ватмана. Появятся чёрные буквы.
Объяснение опыта: При нагревании серная кислота теряет воду и обугливает бумагу.
Ведущие вместе:
Наш вечер удивительных открытий завершён,
он дал вам знания и кучу положительных эмоций.
Желаем всем вам мыслить, фантазировать, творить,
Не закрывать окно в огромный химический мир!